Цель. В текущих рекомендациях в случае неполного подавления вируса у ВИЧ-1-инфицированных предлагается без промедления менять схему высокоактивной антиретровирусной терапии (ВААРТ). Обсервационных и крупных рандомизированных исследований такой тактики не проводилось. Мы исследовали последствия промедления с заменой ВААРТ при вирусологической неудаче лечения.
Дизайн и методы. Чтобы оценить влияние времени, которое проходит от выявления неэффективности схемы первого ряда до ее замены, на смертность от всех причин, использованы проспективные данные двух клинических когорт. Учитывался также состав схемы. Поскольку влияние задержки с заменой схемы может зависеть от прогноза (у пациентов с неблагоприятным прогнозом замена может проводиться раньше, чем у пациентов с хорошим прогнозом), для статистической обработки мы использовали пограничную структурную модель, учитывающую времязависимые факторы.
Результаты. В исследование вошло 982 пациента, период наблюдения после неудачи первой схемы терапии составил в целом 3414 человеко-лет. Задержка с заменой терапии была связана с повышенным риском смерти от всех причин у пациентов с неудачей схем, включавших ингибиторы обратной транскриптазы — НОТ (отношение рисков [ОР] на каждые 3 мес. задержки 1,23; 95%-й доверительный интервал [95% ДИ] 1,08—1,40), однако оказывало небольшое протективное действие у пациентов с неэффективностью схем, включавших ингибиторы протеазы (ОР на каждые 3 мес. задержки 0,93; 95% ДИ 0,87—0,99).
Выводы. Промедление с заменой терапии в случае неудачи схем, не содержащих ингибиторы протеазы, повышает смертность. В случае схем с ингибиторами протеазы влияние задержки с заменой ВААРТ менее значимо. Необходимы действия, направленные на более быструю замену терапии в странах с нехваткой ресурсов, где большинство пациентов начинают ВААРТ со схем на основе ИОТ, а мониторинг вирусной нагрузки не всегда доступен.
Сокращения: 95% АИ — 95%-й доверительный интервал; ВААРТ — высокоактивная антиретровирусная терапия; ИОТ — ингибиторы обратной транскриптазы; МКИ — межквартильный интервал; НИОТ — нуклеозидные ингибиторы обратной транскриптазы; ННИОТ — ненуклеозилные ингибиторы обратной транскриптазы; ОР — отношение рисков.
Введение
В настоящее время в ходе ВААРТ рекомендуется тщательно следить за уровнем РНК ВИЧ в плазме, чтобы как можно раньше выявлять вирусологическую неудачу лечения и при ее подтверждении менять схему терапии. Эта рекомендация имеет две предпосылки: во-первых, репликация вируса усиливает повреждение иммунной системы, в основном, за счет снижения числа лимфоцитов CD4; во-вторых, продолжающаяся репликация вируса способствует накоплению мутаций лекарственной устойчивости, которые ограничивают выбор препаратов в дальнейшем.2
Однако на практике замена неэффективной схемы ВААРТ может откладываться из-за запоздалого выявления вирусологической неудачи, отсутствия планового наблюдения пациента или недоступности альтернативных препаратов. Доступность ВААРТ быстро растет в Африке и других странах с нехваткой ресурсов, в которых распространенность ВИЧ-инфекции очень высока.3 Возможности лабораторной диагностики и инфраструктура здравоохранения в этих странах не позволяют проводить мониторинг вирусной нагрузки, что влечет за собой большие задержки с заменой терапии в случае ее неэффективности.4 8 Чтобы в этих условиях предпринять необходимые меры, нужно изучить отдаленные последствия задержек с заменой терапии.
Теоретически задержка с заменой неудачной схемы первого ряда будет повышать смертность, однако долгосрочных данных, подтверждающих это, недостаточно. Кроме того, есть основания полагать, что последствия задержки замены терапии могут различаться в зависимости от того, включает ли схема ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) либо ингибиторы протеазы. Мутации устойчивости к ингибиторам протеазы (в особенности к усиленным рито-навиром) обычно не возникают быстро при вирусологической неудаче и не всегда приводят к перекрестной устойчивости к всему классу препаратов.914 Кроме того, мутации устойчивости к ингибиторам протеазы в большей степени снижают жизнеспособность вируса, чем мутации устойчивости к другим классам препаратов.1516 Возможно, по этой причине схемы с ингибиторами протеазы часто поддерживают стабильный уровень лимфоцитов CD4 даже при вирусологической недуаче.17,18
Самый верный способ выяснить влияние ранней и отсроченной замены терапии на отдаленные исходы — рандомизировать пациентов на эти две тактики лечения. Однако такая рандомизация неприемлема, т.к. текущие рекомендации и опыт говорят о том, что промедление с заменой терапии приводит к накоплению мутаций лекарственной устойчивости. В отсутствие рандомизированных исследований данные можно получить в проспективных обсервационных исследованиях с четко установленными клиническими когортами. У этого подхода есть недостатки, связанные с время-зависимыми факторами, влияющими на решение о замене терапии. Например, прогрессирование болезни на фоне недостаточного подавления вируса (снижение числа лимфоцитов CD4) может ускорить решение о замене терапии; в результате среди пациентов с отложенной заменой терапии может оказаться больше лиц с медленным прогрессированием болезни, что приведет к ошибочному выводу о защитном эффекте отсроченной замены терапии. Стандартные статистические методы не могут учесть влияние таких факторов, поскольку прогностические факторы во время неэффективной терапии могут сами находиться под ее влиянием.19
В этой работе мы использовали проспективные когортные данные для оценки влияния, которое оказывает задержка с заменой вирусологически неэффективной схемы ВААРТ первого ряда на риск смерти, а также различий этого влияния у разных схем терапии. Дополнительно оценивалась иммунологическая неудача лечения. Для статистического анализа мы применили пограничную структурную модель, которая позволяет учитывать времязависимые факторы.20 Пригодность такого подхода была продемонстрирована в отношении разных областей медицины, и в частности ВИЧ-инфекции.2125
Методы
Дизайн и участники исследования
Данные для анализа получены в двух проспективных когортах: клиники Джонса Хопкинса (JHHCC) и больницы Университета Северной Каролины (UNCHCC). В обеих когортах после получения информированного согласия собиралась информация обученным персоналом. Кроме того, проводился электронный поиск данных из нескольких источников.
В анализ включены пациенты, которые начали ВААРТ за период наблюдения и у которых возникла вирусологическая неудача лечения. Под ВААРТ понимали одно из следующего: любая схема, включавшая 4 антиретровирусных препарата и более; любая схема из 3 препаратов, включая препараты двух или более классов; любая схема, содержащая ингибитор протеазы, усиленный ри-тонавиром, схема из 3 нуклеозидных ингибиторов обратной транскриптазы (НИОТ), содержащая зидовудин/ламивудин/абакавир или зидовудин/ламивудин/ тенофовир.
Вирусологической неудачей считали уровень РНК ВИЧ выше определяемого в двух последовательных измерениях, при этом второе измерение вирусной нагрузки должно было проводиться после 16-й недели. В период между 12-й и 24-й неделей пороговым считался уровень РНК ВИЧ 1000 копий/мл, а после 24-й недели — 500 копий/мл. Учитывались неудачи ВААРТ, выявленные в период с февраля 1996 г. по май 2006 г.
Предметом изучения было время от выявления неэффективности схемы терапии до ее замены. Заменой терапии считали начало лечения новой схемой ВААРТ, содержащей или новый класс препаратов, или хотя бы 2 препарата, не входивших в прежнюю схему. Проведено цензурирование по прерыванию лечения и по его замене.
Основными оцениваемыми показателями были время до смерти от любой причины идо иммунологической неудачи лечения, под которой понимали снижение числа лимфоцитов CD4 ниже исходного уровня в двух последовательных измерениях или в течение любого 12-недельного периода (последний вариант использовался нами в предыдущих исследованиях18и обсуждался в рекомендациях DHHS26).
Статистический анализ
В первичный анализ вошли все отобранные пациенты. Мы провели также два дополнительных анализа, из которых были исключены пациенты с неудачей схем, включавших не усиленные ритонавиром ингибиторы протеазы, а также пациенты, получавшие антиретровирусные препараты до начала ВААРТ. Анализ был также продублирован у лиц со вторым эпизодом вирусологической неудачи.
В качестве времязависимых факторов, которые могли повлиять на результаты, были учтены число лимфоцитов CD4, наименьшее число лимфоцитов CD4, процент лимфоцитов CD4, уровень РНК ВИЧ в плазме и пиковый уровень РНК ВИЧ. Были суммированы такие данные прошлого и текущего анамнеза по ВААРТ, как количество препаратов каждого класса, принимавшихся ранее, и число классов препаратов в текущей схеме. В качестве дополнительного фактора учитывалась также календарная дата. В число исходных и демографических данных вошли пол, возраст, раса, потребление наркотиков, гомосексуальные контакты у мужчин, дата начала ВААРТ и сведения о приеме антиретровирусных препаратов до ВААРТ. Анализ когорты UNCHCC также включал число и процент лимфоцитов CD8, диагностированные болезни из числа критериев СПИДа, дату постановки диагноза ВИЧ-инфекции, а в когорте JHHCC учитывалась дата первого приема антиретровирусных средств. Такой же набор времязависимых и исходных факторов рассматривался в качестве потенциальных предикторов цензурирования, модификации схем терапии и прекращения ВААРТ.
Данные были проанализированы по дискретной временнбй шкале с шагом 1 мес., начиная со времени подтверждения вирусологической неудачи. Значения времязависимых факторов отражали самые последние измерения, имевшиеся на последний день месяца. Все времязависимые факторы были взяты с задержкой 1 мес., чтобы учесть влияние предшествующих величин на решения, касающиеся ВААРТ.
Для воспроизведения результатов исследования, в котором пациенты с неудачей ВААРТ продолжали бы получать прежнюю схему до ее замены на новую в течение рандомизированного периода времени, использован пограничный структурный анализ.19-20-24 Оценки основывались на величинах, обратно пропорциональных взвешенности лечения. В этом случае пациентам приписывались взвешенные величины, обратно пропорциональные вероятности получения прежнего лечения с учетом имевшихся у них ковариат. Созданная таким образом новая взвешенная популяция содержала группы лечения, сбалансированные по распределению ковариат, и была использована в модели взвешенного риска Кокса (или обобщенной логистической регрессии). Взвешенные величины применялись для контроля факторов, вмешивающихся в задержку замены терапии, систематической ошибки в результате информативного цензурирования и прерывания лечения и исходных различий между пациентами, схемы которых содержали и не содержали ингибитор протеазы.20 Все взвешенные величины были стабилизированы.
Взвешенная модель была применена в логистической регрессии, в которой модель выбора основывалась на алгоритме удаления/замены/добавления и 5-кратной перекрестной валидации.27 Этот гибкий подход допускает адаптивный отбор эффектов нелинейных ковариат, взаимодействий ковариат и вариаций во времени. Все взвешенные модели оценивались отдельно для двух когорт, допуская гетерогенность в принятии решений о лечении, вероятности цензурирования и прерывании лечения в зависимости от ковариат между пациентами с неудачей схем с ингибиторами протеазы и пациентами с неудачей схем с ИОТ. Анализ чувствительности выполнен с использованием нескольких альтернативных взвешенных моделей.
После рассмотрения взвешенных величин когорты были объединеныдля общей оценки. В основном анализе мы использовали взвешенную обобщенную логистическую регрессию, в которой в качестве основных параметров выступали время неэффективности терапии и время до ее замены. Мы применили также несколько гибких подходов к моделированию рисков смерти, в т.к. взвешенную адаптивную регрессию с использованием алгоритма удаления/замены/добавления. Для оценки стандартного отклонения применялась непараметрическая бутстреп-выборка.
Результаты
Хотя бы одна вирусологическая неудача ВААРТ развилась у 608 пациентов из когорты JHHCC и 374 пациентов из когорты UNCHCC. В совокупности период наблюдения этих 982 пациентов составил 3414 человеко-лет, медиана — 36,5 мес. на человека (межквартальный интервал [МКИ] 12—70). 742 (76%) случая первой неудачи ВААРТ возникли у пациентов, получавших хотя бы один ингибитор протеазы; из них 234 (32 %) применяли ингибитор протеазы, усиленный ритонавиром. Большинство остальных пациентов (225/240, 94%) получали схемы на основе ННИОТ, из них 163 (72%) — эфавиренз.
В анализ вошли данные всех 982 пациентов; цензурирование проводилось по выбытии из наблюдения, прерывании терапии или смерти, в зависимости от того, что наступило первым. После неудачи ВААРТ у 567 (58%) пациентов схема терапии была изменена; у остальных больных лечение было прервано (п = 286, 29 %), наступила смерть (п = 6, 1 %), или они выбыли из исследования (п = 123, 13%) до замены терапии. Медиана времени от неудачи лечения до замены ВААРТ составила 8 мес. (МКИ 3-19).
За период исследования умерло 93 пациента и наступило 243 иммунологических неудачи лечения. Смертность среди пациентов с неудачей схем на основе ингибитора протеазы и схем на основе ИОТ была одинаковой (2,7 на 100 человеко-лет). Частота иммунологических неудач составила 7,8 на 100 человеко-лет у пациентов, получавших схемы с ингибиторами протеазы, и 10,3 — у поучавших схемы с ИОТ. У 355 пациентов возникла вторая неудача ВААРТ. После нее эти пациенты наблюдались в целом в течение 1014 человеко-лет (медиана 30 мес. на человека, МКИ 20—55). После второй неудачи ВААРТ умерло 36 пациентов и наступило 107 иммунологических неудач.
По сравнению с пациентами с неудачей лечения ИОТ у пациентов с неудачей первой ВААРТ, включавшей ингибиторы протеазы, неудача наступала раньше по календарной дате (р < 0,001), была больше вероятность получения антиретровирусных средств до начала ВААРТ (р < 0,001), схемы на момент неудачи содержали меньшее число НИОТ (р < 0,001); кроме того, наименьшее число лимфоцитов CD4 и текущий уровень лимфоцитов CD4 на момент неудачи были ниже (табл. 1). Средняя вирусная нагрузка до замены ВААРТ составила 3,54 log10 копий/мл у пациентов, получавших ингибиторы протеазы, и 3,7 log10 копий/мл — без них(р = 0,14).
Вероятность замены терапии после первой неудачи была выше у пациентов с низким текущим и минимальным числом лимфоцитов CD4 и высокой вирусной нагрузкой (табл. 2). В когорте JHHCC вероятность замены ВААРТ была ниже, если схема содержала больше препаратов, больше разных классов препаратов или препарат, усиленный ритонавиром. В когорте UNCHCC вероятность замены ВААРТ была выше у пациентов, у которых когда-либо было диагностировано заболевание из числа критериев СПИДа. Такие же тенденции обнаружены после второй неудачи ВААРТ.
Влияние времени замены терапии на смертность и иммунологические неудачи
У пациентов с первой неудачей ВААРТ при лечении ИОТ 3-месячная задержка с заменой терапии повышала риск смерти и иммунологической неудачи (ОР 1,23, 95% ДИ 1,08—1,40, р = 0,002 и ОР 1,21, 95% ДИ 1,07-1,36, р = 0,002 соответственно) (табл. 3). У пациентов с первой неудачей лечения ингибиторами протеазы 3-ме-сячная задержка с заменой терапии немного снижала риск смерти (ОР 0,93, 95% ДИ 0,87-0,99, р = 0,03 vs ОР 0,98, 95% ДИ 0,94—1,03, р = 0,45 при иммунологической неудаче). Однако эти данные нужно трактовать с осторожностью, учитывая множественность проведенных сравнений. Такие же результаты были получены в когортах по отдельности и при анализе второй неудачи ВААРТ (рис. 1).
Таблииа 1. Характеристики выборки на момент первой неудачи ВААРТ
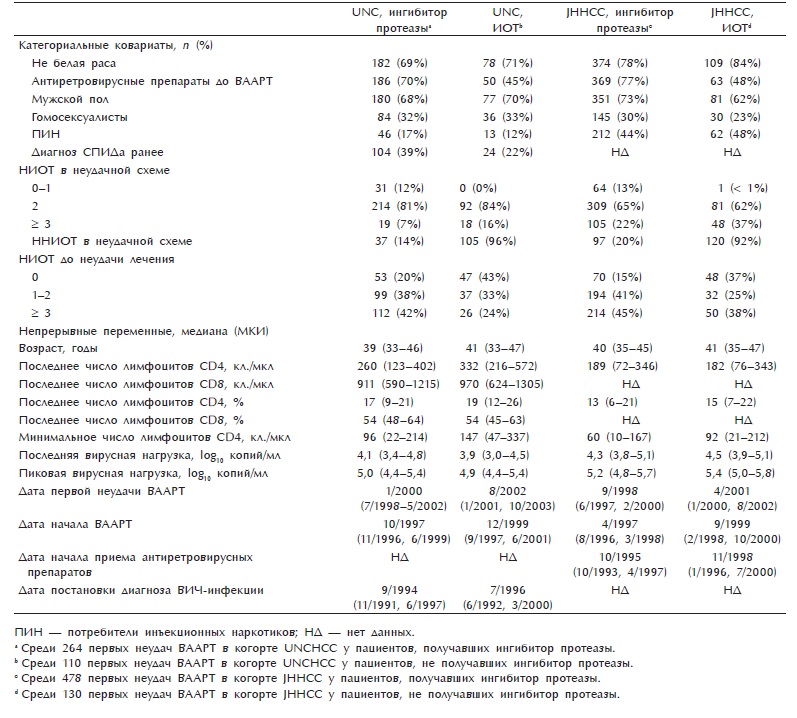
Таблица 2. Связь ковариат с модификацией первой неудачной схемы ВААРТа
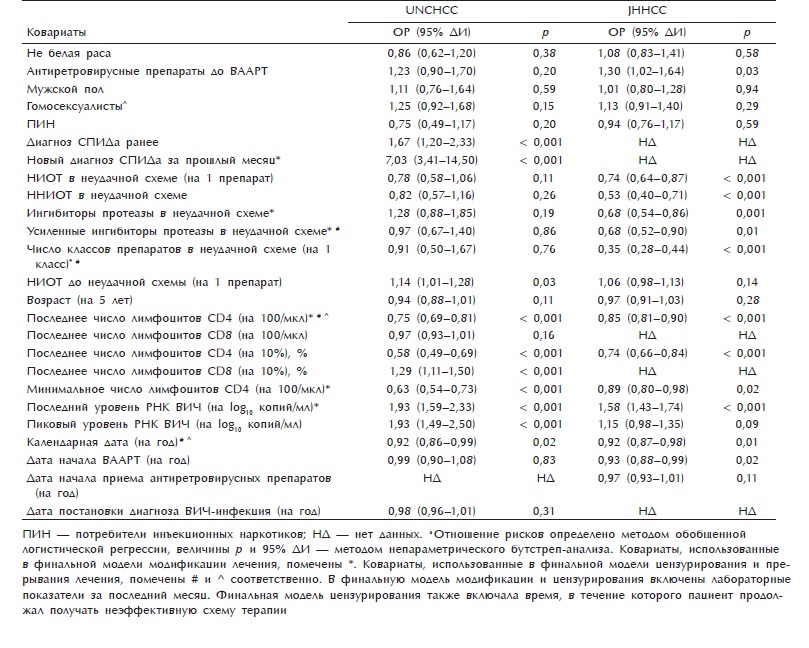
ПИН — потребители инъекционных наркотиков; НД — нет данных. аОтношение рисков определено методом обобшенной логистической регрессии, величины р и 95% ЛИ — методом непараметрического бутстреп-анализа. Ковариаты, использованные в финальной модели модификации лечения, помечены *. Ковариаты, использованные в финальной модели цензурирования и прерывания лечения, помечены # и л соответственно. В финальную модель модификации и цензурирования включены лабораторные показатели за последний месяц. Финальная модель цензурирования также включала время, в течение которого пациент продолжал получать неэффективную схему терапии
Дополнительный анализ и анализ чувствительности
Дополнительный анализ с использованием альтернативных методов оценки взвешенных величин, исключая пациентов, получавших схемы с ингибиторами протеазы без усиления ритонавиром, не выявил существенных изменений результатов (данные не приводятся).
После исключения пациентов, получавших антиретровирусные препаратыдо начала ВААРТ, были проанализированы 187 неудач схем с ингибиторами протеазы и 127 неудач схем с ИОТ. Отношение рисков, связанное с 3-месячной задержкой замены лечения, в этой подгруппе пациентов в целом было таким же, как в основном анализе, хотя разница утратила статистическую значи-мость(при неудаче ИОТ: ОР смерти 1,17, 95% ДИ 0,70— 1,93, ОР иммунологической неудачи 1,07, 95% ДИ 0,85—1,35; при неудаче ингибиторов протеазы: ОР смерти 0,93,95% ДИ 0,69—1,24, ОР иммунологической неудачи 0,95, 95% ДИ 0,85—1,05). На рис. 2 показаны
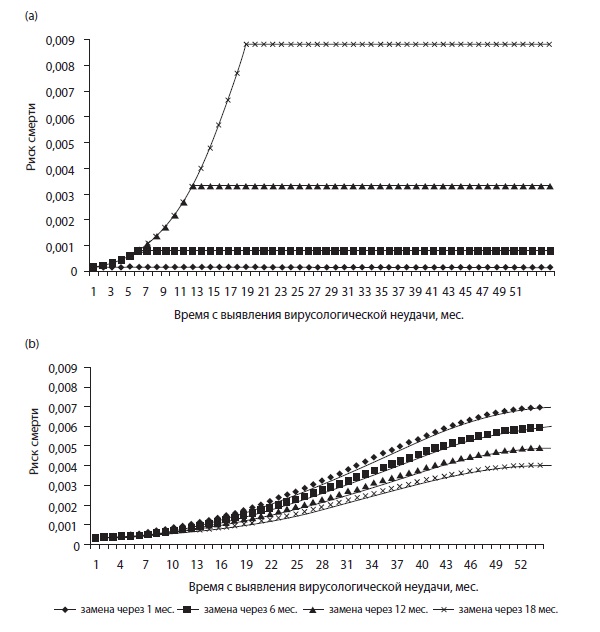
Таблица 3. Относительный риск смерти и иммунологической неудачи ВААРТ в зависимости от задержки замены терапии в случае первой и второй вирусологической неудачи
Оценки получены методом взвешенной обобщённой логистической регрессии. Величины 95% ДИ и р получены методом непараметрического бутстреп-анализа. Под иммунологической неудачей понимали число лимфоцитов CD4 ниже исходного в двух последовательных измерениях или в двух измерениях, сделанных в течение 12 нед.
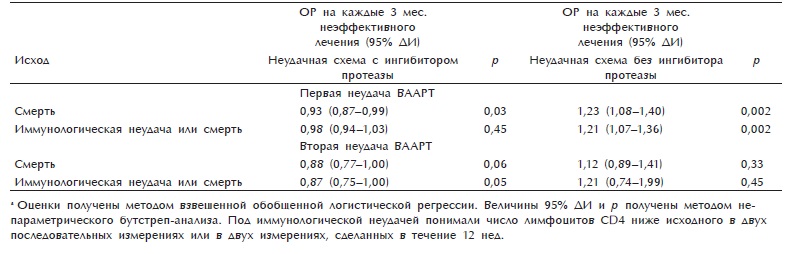
Рис. 1. Отношение рисков, связанное с задержкой замены лечения, в когортах. Оценки получены методом взвешенной обобщенной логистической регрессии. Отношение рисков для схем с ИОТ в когорте UNCHCC после второй неудачи ВА-АРТ не указано в связи с малым размером выборки (п = 31). ИП — неудачная схема с ингибитором протеазы; не-ИП — неудачная схема, не содержавшая ингибиторов протеазы; смерть — смертность от всех причин; неудача по CD4 — составной показатель по смертности от всех причин и иммунологической неудаче; 1-я неудача JHHCC/2-я неудача JHHCC — среди пациентов из когорты JHHCC с первой или второй неудачей ВААРТ соответственно; 1-я неудача UNC/2-я неудача UNC — среди пациентов из когорты UNCHCC с первой или второй неудачей ВААРТ соответственно
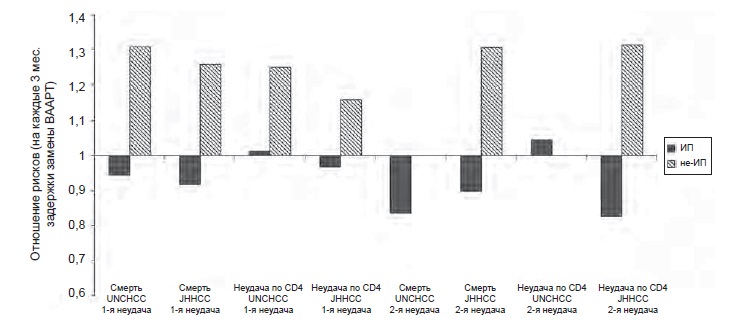
Рис. 2. Риск смерти после первой неудачи ВААРТ в зависимости от времени замены терапии. Оценки получены методом взвешенной обобщенной логистической регрессии. Аля моделирования риска смерти от всех причин использован алгоритм удаления/замены/добавления, (а) Пациенты с неудачей схем с ингибитором протеазы. (Ь) Пациенты с неудачей схем с ИОТ результаты оценки взаимосвязи между временем замены лечения и риском смерти, которая проводилась с использованием альтернативного моделирования.
Обсуждение
При подтверждении вирусологической неудачи в текущих рекомендациях по ВААРТ предлагается менять схему терапии как можно раньше, особенно при неудачах схем первого и второго ряда. Эта рекомендация основана, главным образом, на известных теоретических принципах, однако в обсервационных и крупных рандомизированных исследованиях не изучалась. Проведя подробный анализ времязависимых ковариат в двух крупных когортах, мы обнаружили, что у пациентов с неудачей схем на основе ПОТ (большинство получали ННИОТ и два НИОТ) задержка с заменой терапии в случае вирусологической неудачи повышала риск смерти и иммунологической неудачи в отдаленном периоде. В отношении схем с ингибиторами протеазы повышения риска не отмечено. Такие же результаты были и в дополнительном анализе, ограниченном пациентами, которые до ВААРТ не получали никаких антиретровирусных средств, а также пациентами, которые применяли только ингибиторы протеазы, усиленные ритонавиром.
Для оценки изменения риска смерти со временем в зависимости от срока замены терапии использована адаптивная регрессия. После первой неудачи схем с ИОТ риск смерти резко возрастал, пока пациент продолжал получать неэффективную схему терапии. После замены схемы у пациентов с отложенной заменой терапии риск смерти достигал плато, но оставался повышенным до 4 лет. Этому можно дать два объяснения: во-первых, продолжавшаяся репликация вируса усилила повреждение иммунной системы и повысила риск смерти, а во-вторых, задержка с заменой терапии приводила к накоплению дополнительных мутаций лекарственной устойчивости, что отрицательно сказывалось на дальнейшем лечении.
В отношении схем с ингибиторами протеазы, напротив, отрицательного влияния задержки замены ВААРТ первого или второго ряда не наблюдалось. Адаптивная регрессия подтвердила разницу в риске смерти между этой группой и пациентами, получавшими ИОТ. После первой неудачи ВААРТ с ингибиторами протеазы риск смерти увеличивался со временем, при этом разница в краткосрочной смертности между сменившими лечение сразу и с задержкой была очень небольшой. Снижение риска смерти в случае отложенной замены терапии отмечено только через несколько лет после неудачи лечения.
Отсутствие неблагоприятного эффекта отложенной замены терапии в случае неэффективности ингибиторов протеазы может объясняться несколькими факторами. Во-первых, прежние работы показали, что в случае неэффективности ННИОТ устойчивость развивалась быстро, однако при неэффективности большинства схем на основе ингибиторов протеазы она наблюдалась нечасто.914 Во-вторых, при первой и второй неудаче ВААРТ перекрестная устойчивость к ингибиторам протеазы развивалась реже, чем к ННИОТ. Это означает, что у пациентов с устойчивостью к одному ингибитору протеазы может сохраняться чувствительность к другим препаратам этого класса. Третий, более спорный механизм касается вирулентности устойчивых к ингибиторам протеазы штаммов ВИЧ. При неудаче схем с ингибиторами протеазы число лимфоцитов CD4 снижалось медленнее, чем у схем с ННИОТ.17,28 Это может быть связано как с низким уровнем РНКВИЧ, так и уменьшением способности устойчивого к ингибиторам протеазы штамма вызывать снижение числа лимфоцитов CD4 in vivo.29,30 Наши наблюдения о различиях исходов в зависимости от состава схемы ВААРТ (ННИОТ или ингибитор протеазы) подкрепляются данными исследования, показавшего, что устойчивость к ННИОТ — более стабильный предиктор смертности, чем устойчивость к препаратам других классов.25,31 В целом эти наблюдения свидетельствуют, что при лечении схемами с ингибиторами протеазы болезнь прогрессирует медленнее, чем при лечении схемами с ННИОТ, в ситуациях, когда замена лечения откладывается из-за невозможности выявления вирусологической неудачи (вследствие отсутствия мониторинга вирусной нагрузки) или из-за недоступности схем для замены.
Учитывая обсервационный характер данных, результаты могут быть искажены из-за неучтенных факторов. Важно, однако, что и JHHCC и UNCHCC включили лабораторные данные по усмотрению клиницистов, предоставив доступ к важным сведениям, которые влияют на решение врача о проведении терапии. Дополнительная систематическая ошибка может возникнуть из-за погрешностей моделей, использованных для оценки. Чтобы свести к минимуму влияние этой ошибки, мы применили гибкие адаптивные подходы к моделированию и проанализировали чувствительность, рассмотрев альтернативные модели. Этот дополнительный анализ подтвердил полученные результаты.
Чтобы понять, насколько широко можно обобщать полученные данные, нужно учесть ряд факторов. Во-первых, выявление вирусологической неудачи, от которого зависел набор участников, было обусловлено измерением последовательных уровней РНКВИЧ. Таким образом, у лиц, у которых вирусную нагрузку измеряли чаще, вирусологическая неудача лечения могла определяться быстрее. Точно также выявление иммунологической неудачи зависело от частоты измерений числа лимфоцитов CD4. Кроме того, значительную часть нашей выборки составляли пациенты, применявшие не усиленные ингибиторы протеазы, а также пациенты, получавшие антиретровирусные препараты до начала ВААРТ. Это может ограничивать применимость полученных результатов к условиям широкого доступа к ВААРТ для не-леченных пациентов. Для проверки последнего вопроса мы провели анализ чувствительности, в котором исключили пациентов, применявших до ВААРТ антиретровирусные препараты. Хотя уменьшенный размер выборки означает повышенную вариабельность оценок и утрату статистической значимости, достаточно устойчивое распределение оценок в подгруппах свидетельствует о том, что полученные величины не являются одним лишь результатом антиретровирусного анамнеза у наблюдавшихся когорт пациентов.
Хотя мы не обнаружили очевидного вреда задержки замены ВААРТ у пациентов с неудачей схем с ингибиторами протеазы, следует подчеркнуть, что оптимальные отдаленные клинические исходы наблюдались у пациентов, получавших ИОТ (большинство из которых содержали стандартные ННИОТ и НИОТ) и у которых при неудаче терапии схемы были своевременно заменены. Другими словами, в порядке убывания эффективности в контексте неудачи первой схемы ВААРТ наименьшая смертность отмечена у пациентов с неудачей ИОТ и немедленной заменой терапии, за ними следуют больные с неудачей ингибиторов протеазы с разной отсрочкой заменой терапии, а наибольшая смертность зарегистрирована у пациентов с неудачей ИОТ и задержкой замены терапии.
В целом полученные результаты подкрепляют рекомендации о немедленной замене терапии в случае неудачи схемы первого ряда. Это особенно важно для пациентов, получающих стандартные схемы ВААРТ первого ряда с НИОТ и ННИОТ. С быстрым ростом доступа к ВААРТ во всем мире схемы первого ряда с большой вероятностью будут содержать ННИОТ. Учитывая повышенный риск смерти в случае промедления с заменой таких схем при их неудаче, требуется повысить доступность мониторинга вирусной нагрузки. Наши данные также показывают, что благоприятный эффект ингибиторов протеазы в случае вирусологической неудачи может остаться нереализованным в регионах, где доступ к этим препаратам ограничен.17,18,32,33 Это следует учесть при планировании поставок препаратов и предпринять меры по сокращению задержек с заменой терапии в случае ее неэффективности.