Резекцию пищевода по методу Добромыслова — Торека мы применяем у тех больных, которым до операции поставлен диагноз рака пищевода III стадии при локализации опухоли на любом уровне грудного отдела, кроме нижнего.
Подходим к пищеводу всегда со стороны правой плевральной полости.
Операцию Добромыслова — Торека мы производим следующим образом.
После блокады правого звездчатого узла и спинномозговой анестезии, о чем подробно сказано в главе IV, больной остается лежать на левом боку с подложенным под грудь валиком и с отведенной вперед и кверху правой рукой. Операционное поле подготавливается обычно. Если опухоль располагается на уровне IV—VI грудных позвонков, то разрез грудной стенки производят по шестому межреберью, если ниже, то по седьмому. Разрез начинают от края длинных мышц спины, ведут строго по избранному межреберью через боковую поверхность груди на переднюю (20—25 см). Грудную клетку вскрывают послойно, кровоточащие сосуды захватывают зажимами. После пересечения межреберных мышц в одном участке рассекают париетальную плевру на 1 см и путем периодического прижатия дефекта в плевре влажной салфеткой достигают постепенного поступления воздуха в плевральную полость. В это же время кетгутовой нитью лигируют все сосуды мышц и подкожной клетчатки. Затем разрез париетальной плевры увеличивают соответственно разрезу кожи и мышц грудной стенки и производят дополнительный гемостаз. Края раны обкладывают марлевыми салфетками и разводят с помощью грудного расширителя. Мы никогда не резецируем и не пересекаем ребер, так как не видим в этом необходимости.
После разведения краев раны становится видна плевральная полость с поджатым к корню легким. Если имеются плевральные спайки или сращения, их рассекают ножницами с боковой и задней поверхностей. Первый помощник осторожно левой рукой приподнимает и отводит легкое вперед. Становится видна медиастинальная плевра и под ней контурируется опухоль пищевода или же видно сращение плевры с карциномой. Рассекают медиастинальную плевру от диафрагмы до дуги непарной вены. Если часть плевры сращена с карциномой, ее оставляют на опухоли. Теперь на 2—3 см ниже опухоли хирург освобождает пищевод кругом и берет его на тесемку-держалку. Если верхний полюс опухоли не доходит до уровня дуги непарной вены на 2—3 см, то вену не пересекают. В противном случае вену обшивают в двух местах, перевязывают и перерезают.
Продолжают рассечение медиастинальной плевры кверху. Выше верхнего полюса опухоли пищевод тоже выделяют кругом и берут на тесемку-держалку (рис. 55). После этого начинается самый основной и ответственный этап операции— выделение пищевода в области опухоли вместе с уплотненной околопищеводной клетчаткой и видимыми лимфатическими узлами. Освобождение пищевода на всем протяжении грудного отдела, в том числе и в области опухоли, хирург производит с помощью ножниц и лишь иногда пользуется тупфером; пальцевое выделение не применяется совершенно. Поворачивать пищевод в ту или другую сторону помогают две тесемки-держалки. Все сосуды, подходящие к пищеводу, обязательно лигируют. Особенно осторожно и внимательно отделяют пищевод от стенки аорты, трахеи, бронхов, если опухоль расположена на этом уровне.
Много внимания требуется для того, чтобы, выделяя опухоль с левой стороны, не ранить левую медиастинальную плевру. Если опухоль сращена с ней, нам, оперирующим под спинномозговым обезболиванием, приходится производить больному сначала интубацию трахеи под местной анестезией, а затем, когда будет налажена подача кислорода под повышенным давлением, иссекать участок левой медиастинальной плевры. Этот момент вскрытия второй плевральной полости мы оставляем на конец операции. После того как опухоль пищевода выделена со всех сторон (или остается фиксированной только к участку левой медиастинальной плевры), производят выделение пищевода вниз до диафрагмы и вверх до шейного отдела.
Над диафрагмой мышечную оболочку пищевода надсекают кругом. Остающийся цилиндр пищевода из слизистой оболочки и подслизистого слоя прошивают в двух местах и завязывают на обе стороны. Проксимальнее второй лигатуры пищевод еще раз прошивают прочной нитью и перевязывают. Теперь пищевод рассекают между лигатурами, культи его смазывают настойкой йода. На конец пищевода, оставшийся на желудке, накладывают 5—6 нитяных узловых швов, погружающих завязанную слизистую. Нити срезают й пищевод погружают под диафрагму.
С грудного отдела пищевода снимают .'держалку, наложенную ниже опухоли, а ту, которая была выше опухоли, прочно завязывают узлом, прекращая доступ слюны в пищевод. Концы тесемки коротко обрезают. Теперь, если левая медиастинальная плевра была сращена с опухолью, после интубации трахеи участок плевры иссекают и мобилизацию пищевода заканчивают полностью.
Пищевод оставляют в средостении. Никаких напалечников на его конец мы не надеваем. В средостение вводят антибиотики. Правую медиастинальную плевру зашивают; если же она иссечена на значительном участке, то зашить ее герметично не удается. Мы не видели какой-либо разницы в течении послеоперационного периода в том и в другом случае. Если операция была длительна и достаточно травматична, то через прокол в девятом межреберье по заднеаксиллярной линии ставится дренажная трубка на 2—3 дня; в противном случае трубка не ставится. Снимают ранорасширитель, зашивают грудную клетку.
Больного поворачивают на спину. Хирурги Делятся на две группы. Двое ведут операцию на шее. Под местной анестезией проводят разрез по внутреннему краю грудино-ключично-сосковой мышцы слева. Рану углубляют до пищевода. Левый возвратный нерв вместе с участком клетчатки отводят крючком внутри. Вводят малые шейные крючки из набора инструментов А. Г Савиных и, если пищевод со стороны грудной полости был выделен достаточно высоко, остается только подтянуть его пинцетом, подвести под него указательный палец правой руки и весь грудной отдел пищевода вместе с опухолью свободно выводится в шейную рану (рис. 56) Чтобы воздух при дыхании не поступал в грудную полость во время дальнейшей операции, мы тампонируем средостение через нижний угол шейной раны влажной салфеткой Пищевод по окружности фиксируют к подкожной клетчатке вблизи грудино-ключичного сочленения (швы проводят через мышечный слой пищевода). Тампон из средостения удаляют и зашивают шейную рану. Только после этого резецируют пищевод, причем сначала пересекают мышечный слой, а после того, как он сократится, несколько дистальнее пересекают слизистую оболочку. При таком пересечении она не уходит в просвет пищевода и легко подшивается к краям кожи — создается пищеводный свищ.
Третий хирург из участников торакотомии вместе с помощником производит лапаротомию в левом подреберье, осматривает кардиальный отдел желудка, малый сальник, печень. После ревизии брюшной полости накладывают гастростому по методу Кадера.
По окончании операции на шее производят аспирацию воздуха из правой плевральной полости (если была ранена левая медиастинальная плевра, то и из левой) через отдельный прокол иглой Дюфо или через дренажную трубку, если она была поставлена. Удаление воздуха производят с помощью шприца Жане. На этом операция заканчивается. Средняя ее продолжительность 21т—3 часа.
Мы считаем целесообразным накладывать желудочный свищ одновременно с операцией резекции пищевода, во-первых, потому, что она производится другой группой хирургов одновременно с операцией на шее, а следовательно, не удлиняет пребывание больного на операционном столе; во-вторых, потому, что эта операция выполняется у нас под еще действующей спинномозговой анестезией, когда и осмотр верхних отделов брюшной полости можно произвести тщательнее, чем под местной анестезией, применяемой для наложения гастростомы, если эта операция выполняется в другое время. Сторонники наложения предварительной гастростомы правы в том, что они в первую очередь выясняют, имеются или нет метастазы рака в брюшную полость и можно ли их убрать. Таким образом, они избегают ненужных резекций пищевода. Однако предварительно наложенная гастростома может иногда повлечь отсрочку основной операции вследствие каких-либо осложнений.
Наложение гастростомы спустя 3—4 дня после резекции пищевода, как это делает Б. А. Петров, не имеет, по нашему мнению, никаких преимуществ перед одномоментным ее наложением. В то же время брать больного с повышенной температурой, у которого иногда имеются осложнения со стороны плевры, легких, на операцию гастростомии нам представляется менее удобным, чем выполнить это в один прием.
Приводим выписки из историй болезни больных оперированных по методу Добромыслова — Торека.
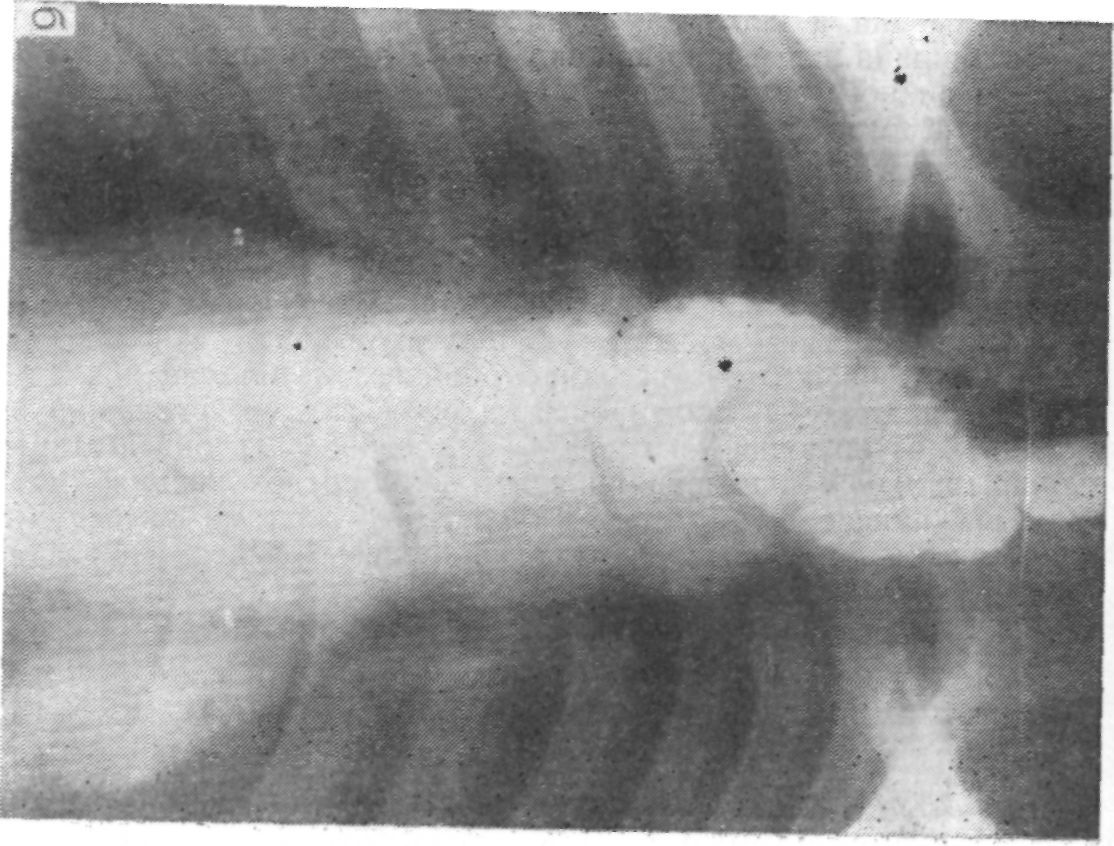
Больной Н„ 47 лет, поступил в клинику 26/Х1 1955 г с жалобами на дисфагию. Считает себя больным 2 месяца сведение удовлетворительное Питание понижено: рост 1/8 см, вес 66,3 кг. При рентгенологическом исследовании установлено, что в средней трети пищевода (уровень VI—VII грудных позвонков) на задней стенке определяется дефект наполнения плоского характера со значительным изъязвлением в центре. Протяженность дефекта до 5—6 см, стенка пищевода здесь не видна. Инфильтрация средостения на этом уровне выражена умеренно (рис. о/). Клинический диагноз: рак средне-грудного отдела пищевода, стадия III.
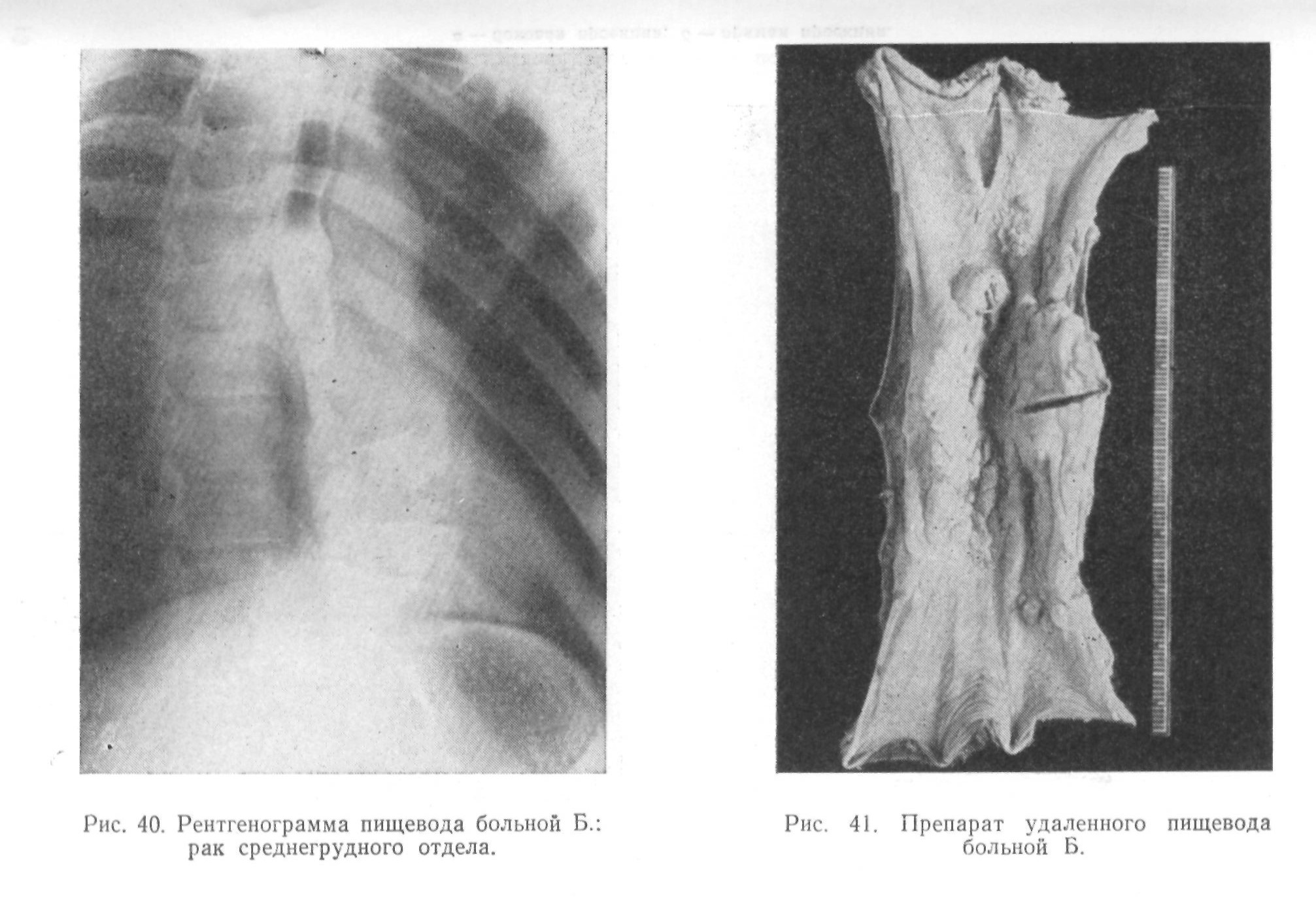
12/ХП произведена резекция пищевода по методу Добромыслова — Торека с образованием пищеводного и желудочного свищей. I рудная полость вскрыта по шестому межреберью справа. Имевшиеся плевральные- спайки пересечены. Несколько ниже непарной вены определялась опухоль пищевода на протяжении 5—6 см, сросшаяся с правой медиастинальной плеврой. Сюда же был припаян край легкого. Небольшой участок легочной ткани был иссечен, дефект в легком зашит. При выделении опухоли пищевода часть правой медиастинальной плевры была резецирована, она осталась на опухоли. Карцинома высекалась из клетчатки средостения с некоторым трудом, так как слева близко прилегала к нисходящей грудной аорте. Лимфатических узлов в средостении не обнаружено. Пищевод выделен на всем протяжении грудного отдела; внизу он пересечен. Грудная полость закрыта послойно. Дренажная трубка не ставилась.
Пищевод обнажен на шее слева, грудной отдел выведен в рану и резецирован. Наложен пищеводный свищ; гасгростома.
Длина удаленного отдела пищевода 16 см. Опухоль в виде язвы занимает 6 см по протяжению пищевода и 4 см в ширину. От опухоли до нижнего края пищевода 4,5 см, до верхнего — 5,5см. Гистологический диагноз: плоскоклеточный ороговевающий рак.
Во время операции, длившейся 3 часа, состояние больного было вполне удовлетворительным. Кровь не переливали.
Послеоперационный период протекал удовлетворительно, однако у больного в течение 8—10 дней был кашель, постепенно прекратившийся; 7/1 1965 г. больной выписан из клиники.
При повторном поступлении в клинику 10/1У 1956 г. больному выполнена операция загрудинно-предфасциальной пластики пищевода. Во время этой операции при тщательном осмотре брюшной полости метастазов обнаружено не было. Послеоперационный период без осложнений; 12/У больной выписан из клиники. В настоящее время чувствует себя хорошо и работает. После резекции пищевода прошло 10 лет.
Приведенное наблюдение свидетельствует о том, что рак пищевода III стадии, вышедший местно за пределы стенки пищевода, сросшийся с медиастинальной плеврой и даже с краем легкого, но не давший метастазов, излечивается благодаря операции иногда довольно стойко и на длительное время.
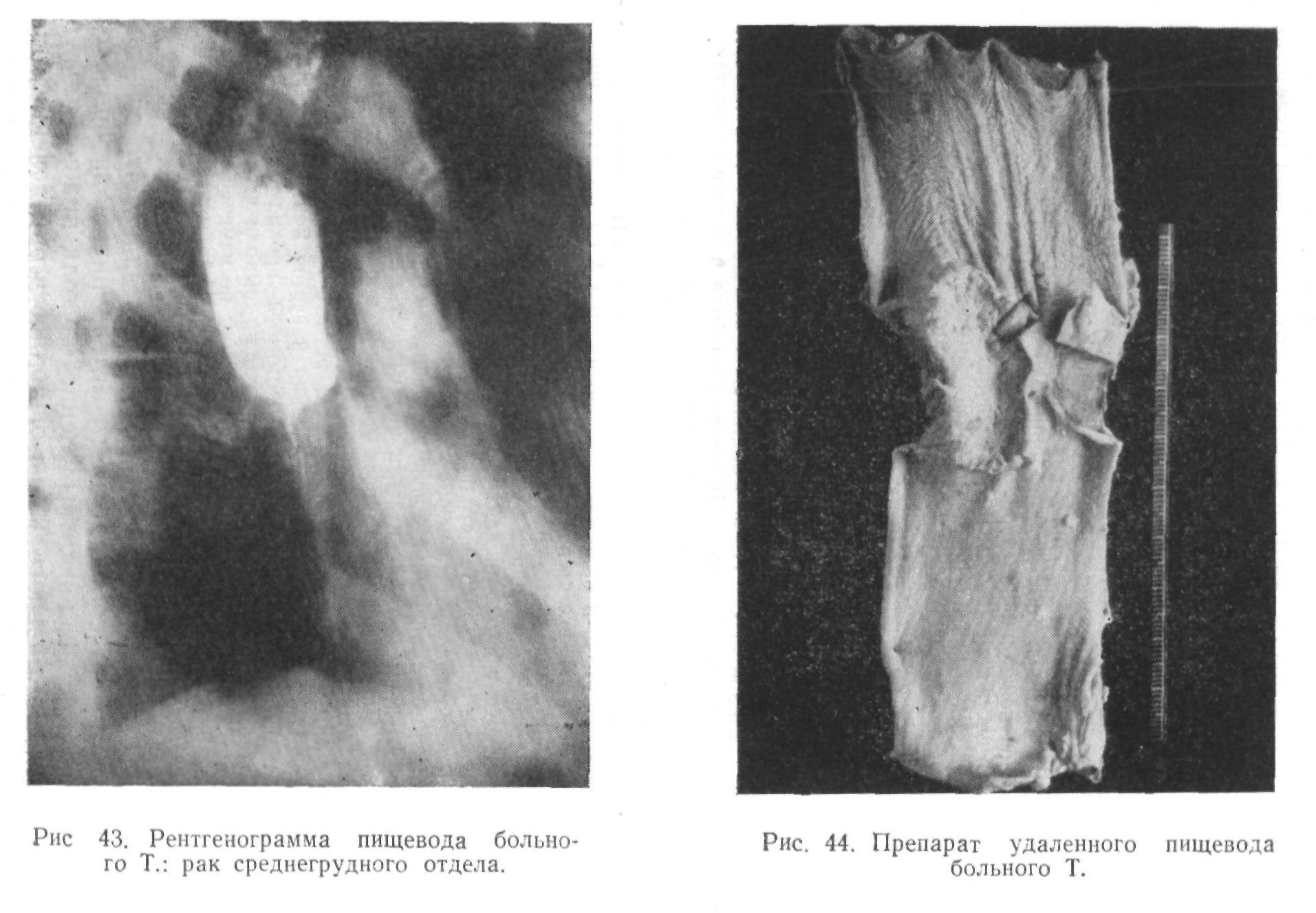
Больной X., 50 лет, поступил в клинику 19/У1 1959 г. с жалобами на дисфагию и постоянные боли в области сердца и левой лопатки. Считает себя больным 3 года, однако пища стала в пищеводе задерживаться 7 месяцев назад.
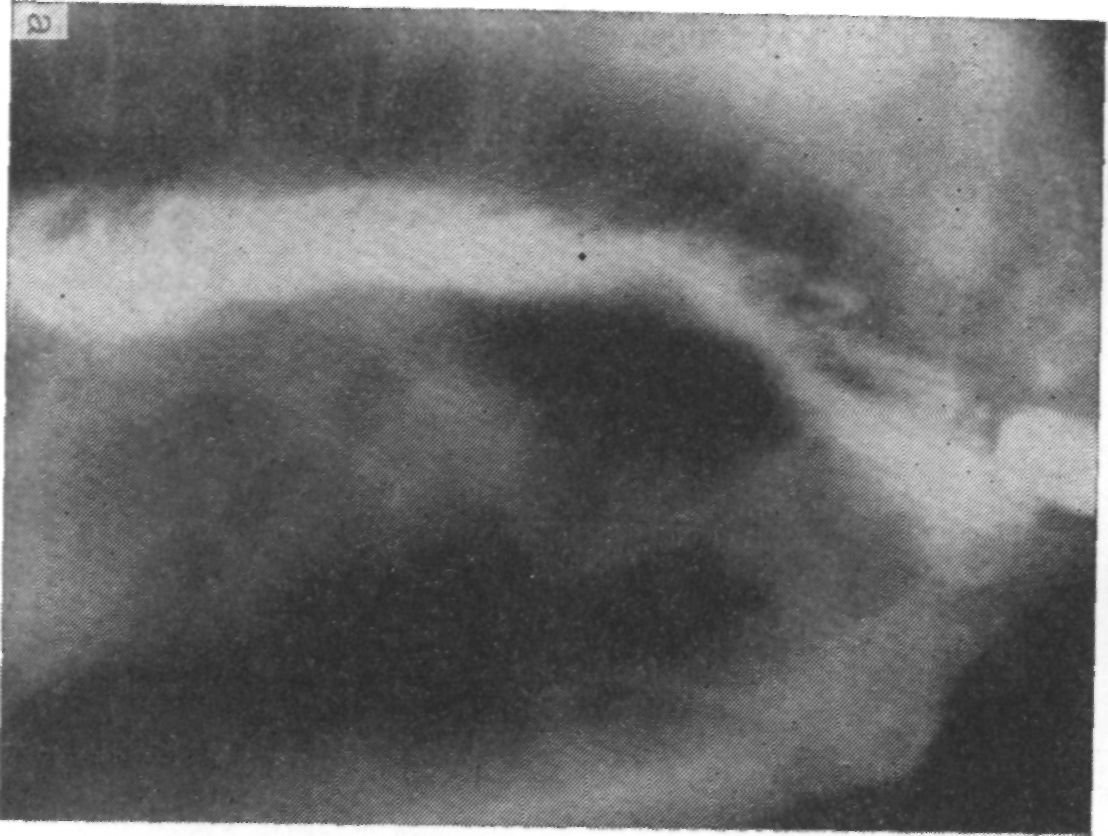
Общее состояние удовлетворительное. Питание понижено: рост 184 см, вес 76 кг. При рентгенологическом исследовании установлено, что жидкая контрастная масса стойко задерживается в пищеводе на уровне VI грудного позвонка и дальше, почти до диафрагмы, идет суженной неровной полосой и в небольшом количестве. В заднем средостении на месте дефекта видна умеренная инфильтрация. Выше сужения пищевод расширен (рис. 59). Клинический диагноз: рак средне- и нижне-грудного отделов пищевода, стадия III.
7/У11 выполнена резекция пищевода по методу Добромыслова — Торека с образованием пищеводного и желудочного свищей. Грудная полость вскрыта по седьмому межреберью справа.
Медиастинальная плевра не вовлечена в процесс, она рассечена от диафрагмы до непарной вены. В пищеводе примерно на 4 см ниже непарной вены определяется опухоль, почти достигающая уровня диафрагмы. При выделении пищевода слева и справа от опухоли было обнаружено по одному увеличенному лимфатическому узлу, они иссечены вместе с опухолью. Пищевод выделялся довольно легко. Внизу он пересечен на границе с кардией. Операция закончилась наложением пищеводного и желудочного свищей. Во время наложения гастростомы при ревизии брюшной полости метастазов не обнаружено. Операция длилась более 3 часов.
Удаленный грудной отдел пищевода имеет длину 18 см. Опухоль в виде язвы занимает 10,5 см пищевода почти циркулярно, кроме заднеправой стенки, где слизистая оболочка сохранена. От опухоли до нижнего конца пищевода 2 см, до верхнего — 5,5 см. Гистологический диагноз: плоскоклеточный не ороговевающий рак. В лимфатических узлах из средостения метастазов не обнаружено.
Послеоперационный период без осложнений: 5/1Х больной выписан из клиники.
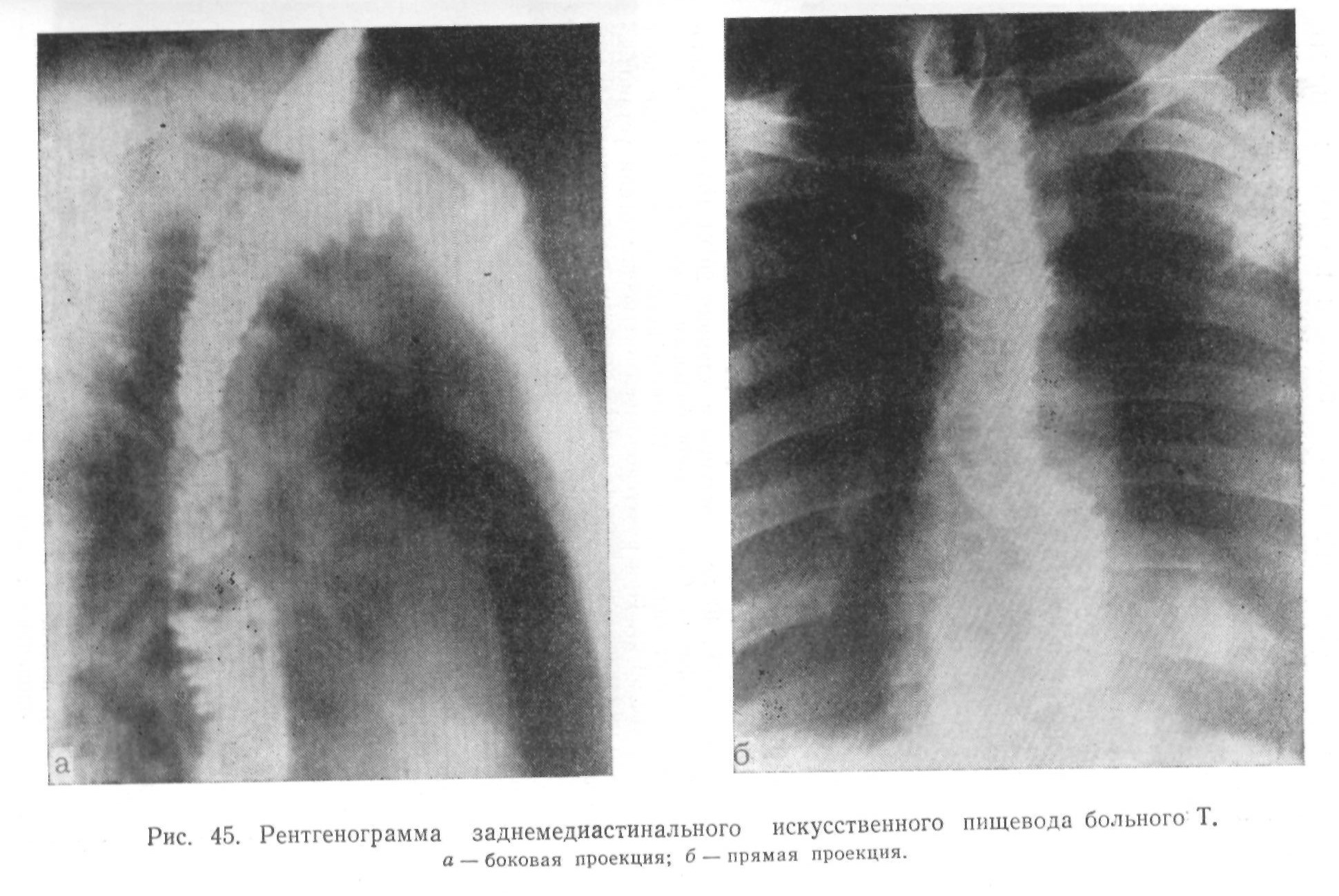
При повторном поступлении 9/П 1960 г. во время лапаротомии метастазов нигде не обнаружено. Сделан загрудинно-предфасциальный искусственный пищевод из тощей кишки.
Третий раз в клинику больной поступил в марте 1961 г. с просьбой соединить искусственный пищевод с желудком. Во время этой операции был обнаружен конгломерат плотных неподвижных лимфатических узлов по ходу левой желудочной артерии; убрать их было невозможно. Больной жил после операции резекции пищевода более 2 лет.
Данное наблюдение показывает, что и большую опухоль пищевода средне и нижне-грудного отделов, если она не срослась с окружающими органами, бывает можно выделить и удалить. Однако конечный результат операции не всегда благоприятен, даже в случаях повторных осмотров брюшной полости и отсутствии видимых метастазов в течение 7 месяцев после резекции пищевода.
Итак, из 130 операций резекции пищевода по методу Добромыслова — Торека выполнено 55 с двумя неблагоприятными исходами (3,6%). У всех больных подход к пищеводу был осуществлен через правую плевральную полость. В 36 наблюдениях правая медиастинальная плевра была вовлечена в процесс и иссекалась вместе с опухолью, причем у 7 больных, кроме плевры, в опухоль был впаян и край правого легкого, который пришлось резецировать. У 3 больных к опухоли были припаяны обе медиастинальные плевры и во время операции обе частично иссечены. Только у 19 больных медиастинальная плевра не была спаяна с опухолью.
На основании приведенных данных можно сказать, что правосторонний подход к опухоли пищевода вполне оправдан. На 55 операций только в 3 случаях возник двусторонний пневмоторакс. Если бы мы шли слева, то он возник бы у 36 больных. Хотя в настоящее время двусторонний пневмоторакс, особенно при интубационном наркозе, не является грозным осложнением, однако такие больные тяжело переносят послеоперационный период и нередко гибнут от сердечно-легочной недостаточности. Таким образом, мы еще раз подтверждаем целесообразность правостороннего чресплеврального подхода к пищеводу.
Из 53 больных, выписавшихся после резекции пищевода по методу Добромыслова — Торека, искусственный загрудинно-предфасциальный пищевод из тощей кишки сделан 38; 11 человек для повторной операции не приехали; 4 больным отказано в операции из-за перенесенной лучевой болезни или обнаружения метастазов.
Какие же преимущества имеет операция резекции пищевода по методу Добромыслова — Торека перед другими? Ее преимуществом перед операцией по Савиных является возможность резецировать пищевод при довольно запущенном раке (в III стадии), при прорастании опухолью медиастинальной плевры.
Преимуществами операции по Добромыслову — Тереку перед одномоментными операциями типа Гарлока и Льюиса является, во-первых, меньшая продолжительность и объем вмешательства, а следовательно, и меньшая травматичность; во-вторых, отсутствие опасного для жизни пищеводно-желудочного анастомоза в плевральной полости; в-третьих, большая радикальность, так как иссекается весь грудной отдел пищевода.
Недостаток операции Добромыслова — Торека, по мнению многих хирургов, состоит в том, что при ней сразу не восстанавливается пищеводно-желудочная или пищеводно-кишечная непрерывность, как при одномоментных операциях. Однако в последние годы операция создания искусственного пищевода настолько усовершенствована, что довольно просто выполняется спустя 1—3 месяца после резекции пищевода. Поэтому операция Добромыслова— Торека, дающая в 2, 3 раза меньшую послеоперационную летальность по сравнению с одномоментными операциями и достаточно радикальная, должна применяться у больных раком III стадии при локализации процесса во всех отделах грудного пищевода, кроме нижнего.
Нам могут возразить, что после резекции пищевода по Добромыслову — Тореку должна быть произведена еще одна операция — пластика пищевода, которая тоже может дать неблагоприятный исход. Совершенно справедливо. Но операция пластики пищевода тонкой кишкой в настоящее время дает минимальную летальность.
А. А. Русанов из 57 больных, которым он сделал пластику по Ру—Герцену — Юдину, не потерял ни одного больного. В. И. Попов и В. И. Филин сообщают, что «летальных исходов после пластики пищевода, произведенной после резекции пищевода по Тореку... не было». У нас не было ни одного неблагоприятного исхода на 56 операций эзофагопластики. Следовательно, операция пластики пищевода после его резекции для жизни не опасна.
Есть еще одно возражение: после операции Добромыслова — Торека часть больных или отказывается от второй операции, или не поступает для ее производства из-за тяжести состояния.
Если операция пластики пищевода не будет давать неблагоприятных исходов, случаев отказа от нее не будет. Мы убедились в этом на примере своих больных. Никто из них не отказывался от операции, а некоторые, наоборот, просили сделать искусственный пищевод как можно скорее.
Вопрос же о том, что часть больных умирает без пластики пищевода, является более серьезным. Он не зависит от наших хирургических возможностей, а всецело подчинен самой болезни. Помочь здесь может, по нашему мнению, только ограничение числа паллиативных резекций (при множественных метастазах). Если же резекция пищевода сделана и выясняется, что она является только паллиативной, то следует скорее приступать к созданию искусственного пищевода: не ждать 3—6 месяцев, как обычно, а, не выписывая больного из стационара, через 4 недели после резекции пищевода создать ему пищеводно-кишечную непрерывность, разумеется, если позволяет общее состояние.
В отношении порядка производства этапов операции, как отмечалось выше, нет единой точки зрения, и нам хотелось бы высказать свои соображения по этому вопросу.
В 1949 г. Н. И. Еремеев на заседании Томского хирургического общества сообщил о своей замечательной операции. Он помещал тонкую кишку — искусственный пищевод — в переднем средостении, анастомозируя ее с пищеводом на шее. Его исследования показали, что при проведении в переднем средостении кишки требуется примерно на 10 см меньше, чем при подкожном проведении. Н. И. Еремеев рекомендовал эту методику как предварительный этап хирургического лечения рака пищевода. А. Г. Савиных операцию создания искусственного пищевода в переднем средостении, разработанную Н. И. Еремеевым под его руководством, стал применять в клинике с 1951 г. у неоперабельных больных раком пищевода и кардии как паллиативное пособие. В 1952 г. А. Г. Савиных сообщил в печати свое первое впечатление об этом вмешательстве. Он писал, что при неоперабельном процессе в пищеводе этот метод как паллиативный заслуживает серьезного внимания. Кроме того, он считал, что это вмешательство следует применять как предварительное при двухэтапных операциях.
В такой последовательности двухэтапную операцию при раке пищевода в клинике впервые удалось выполнить в 1955 г.
Приводим выписку из истории болезни.
Больная Ш., 42 лет, поступила в клинику ЗЦ/1У 1955 г. с жалобами на дисфагию. Считает себя больной 7 месяцев.
Общее состояние удовлетворительное. Питание понижено: рост 154 см, вес 48 кг. При рентгенологическом исследовании установлено, что в пищеводе на уровне VI—VII грудных позвонков определяется циркулярный дефект протяженностью около 4 см. Контуры пищевода в зоне дефекта неровные. Видна лишь незначительная инфильтрация заднего средостения на уровне поражения пищевода (рис. 61). Клинический диагноз: рак среднегрудного отдела пищевода, стадия II.
Начата подготовка к операции резекции пищевода по методу Савиных, произведена лапаротомия, диафрагмокруротомия. При выделении опухоли пищевода обнаружено, что она срослась с правой медиастинальной плеврой. Попытка отделить опухоль повлекла к разрыву плевры. Средостение затампонировано влажной салфеткой. Выполнена загрудинно-предфасциальная эзофагопластика. Сделана гастростомия.
Послеоперационный период без осложнений. На 5-й день больной было разрешено глотать жидкости, на 6-й полужидкую пищу. Проходимость искусственного пищевода была хорошей, что подтверждено 15ДТ при рентгенологическом исследовании.
Несмотря на то 4Го послеоперационный период протекал без осложнений, вторая операция была отложена почти на месяц. У больной, свободно глотавшей любую пищу, не было желания повторно оперироваться, да и общее состояние оставалось тяжелым. Аппетит отсутствовал, отмечалась общая слабость.
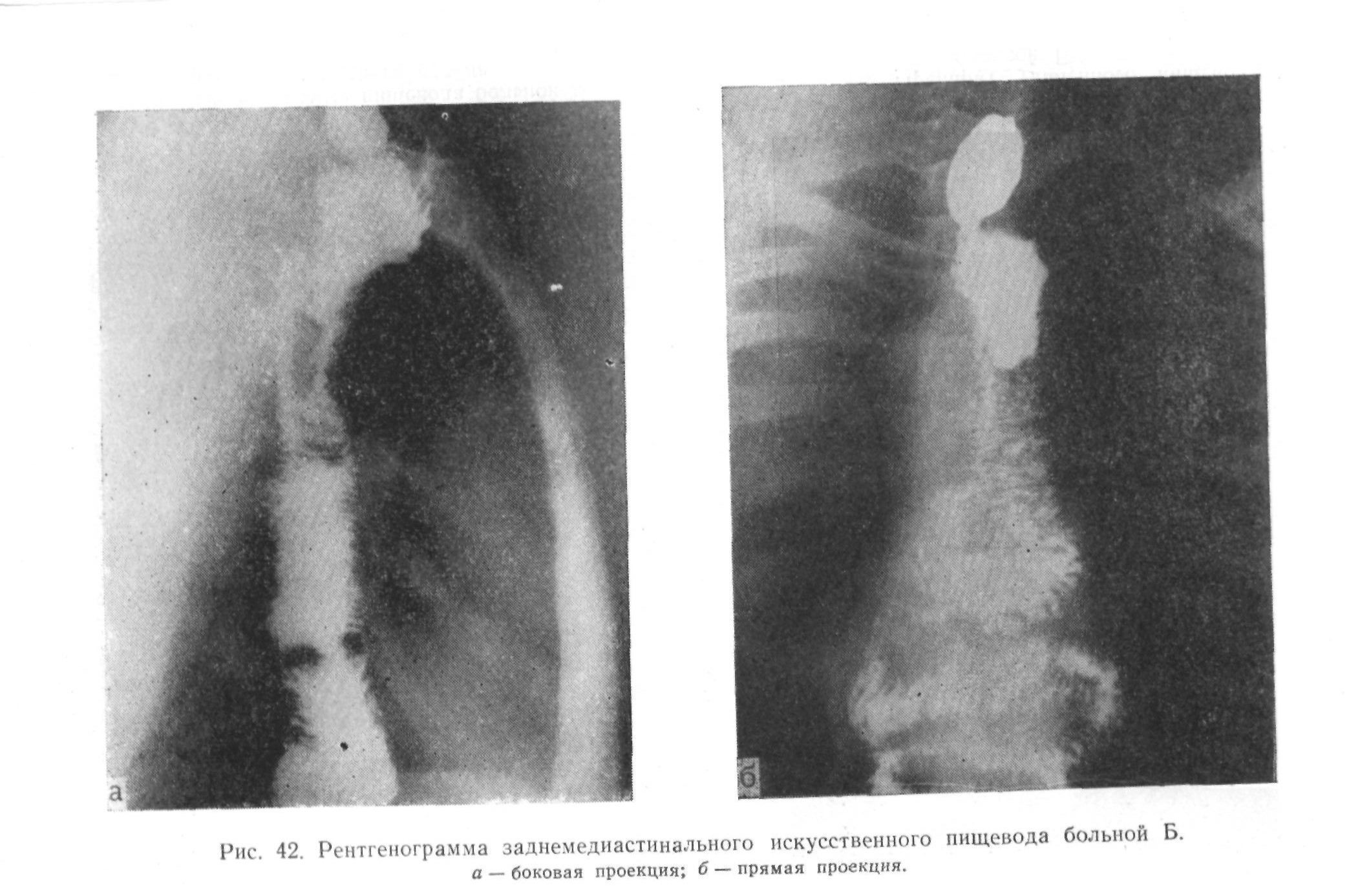
Только 25/У1, после повторной подготовки, мы смогли выполнить резекцию пищевода по методу Добромыслова — Торека. Грудная полость вскрыта по седьмому межреберью справа. В полости плевры небольшое количество серозной жидкости, пленки фибрина как результат бывшей плевротомии. Пищевод в нижнем отделе, где он был освобожден раньше, сейчас выделялся с большим трудом, так же как и в области опухоли, где он был высечен вместе с участком правой медиастинальной плевры и краем правого легкого. Выше опухоли пищевод выделялся легко, за исключением верхнего зашитого конца, вокруг которого были плотные рубцы. После резекции пищевода плевральная полость закрыта без дренажа.
Послеоперационное течение без осложнений. На 5-й день больная начала ходить. Через 55 дней после пластики пищевода был закрыт желудочный свищ; 1/У1Н больная выписана из клиники. Прожила всего 8 месяцев.
У нас не сложилось хорошего впечатления от такой последовательности в выполнении данной операции. Предоперационную подготовку пришлось проводить дважды: перед пластикой и перед резекцией пищевода. К моменту второй ответственной операции резекции пищевода больная была более ослабленной, чем перед первой. Кроме того, и желания оперироваться второй раз, имея возможность свободно питаться через рот, у нее не было. Психическую подготовку таких больных для повторной операции проводить не просто. Кроме того, мы не знаем, как ведет себя злокачественная опухоль пищевода после того, как организм значительно ослаблен серьезным оперативным вмешательством-. У больной Ш. во время обеих операций мы не видели метастазов ни в брюшной полости, ни в средостении. Прожила она всего 8 месяцев после операции. Правда, мы не знаем, точно, от чего она умерла.
Учтя все указанное, в последующей своей работе мы изменили порядок выполнения операции: сначала производим резекцию пищевода по методу Добромыслова — Торека, а спустя 1—3 месяца выполняем загрудинно-предфасциальную пластику. Оперируя в такой последовательности в течение 10 лет, мы считаем ее более правильной.
Операция, предложенная Н. И. Еремеевым, в нашей клинике претерпела некоторые изменения. С 1954 г. по предложению А. Г. Савиных кишечную петлю стали проводить не в переднем средостении между плевральными листками, а загрудинно-предфасциально, т. е. между грудиной и отслоенной внутригрудной фасцией. Это предложение было вызвано желанием уменьшить количество плевротомий, которые часто возникали при создании хода в переднем средостении. Хирурги, оперировавшие по Н. И. Еремееву (Б. А. Петров, П. К. Дьяченко и др.), отмечали, что при образовании хода в переднем средостении очень часто нарушается целость правой медиастинальной плевры, а иногда обоих плевральных листков. При отслойке внутригрудной фасции такие осложнения возникают редко.
А. И. Осипов в анатомической работе показал возможность отслаивать внутригрудную фасцию от грудины без повреждения плевральных листков. В 1957 г. была опубликована работа А. Н. Мачабели, в которой автор описал две операции пластики пищевода из толстой кишки, проведенные тоже загрудинно после отслойки внутригрудной фасции. Он предложил такую операцию называть загрудинной пластикой. У нас в клинике эта операция получила название загрудинно-предфасциальной пластики пищевода.
По мнению Я. В. Волколакова, создание загрудинного хода для пластики пищевода, выполняемое большинством хирургов вслепую, может повлечь повреждение плевры, а проведение кишки в такой канал может вызвать нарушение питания трансплантата вследствие перекручивания кишечной петли или сдавления ее тонкими прочными фиброзными тяжами, которые иногда остаются в загрудинном пространстве. Чтобы избежать этих осложнений, автор предлагает загрудинный ход, созданный вслепую с помощью шпателя его конструкции, расширять после продольного рассечения грудины и укладывать здесь трансплантат под контролем зрения.
Мы уже сообщали свое мнение по поводу продольной стернотомии при загрудинной пластике пищевода (Хирургия, 1965, № 2), основанное на опыте клиники в 145 операций загрудинно-предфасциальной эзофагопластики. Оно состоит в том, что продольное рассечение грудины, являясь дополнительной травмой, усложняющей непростую операцию эзофагопластики, не обосновано и не должно применяться в клинике. В дальнейшем изложении мы постараемся показать, что при методике, используемой нашей клиникой при создании загрудинно-предфасциальной эзофагоплистикн, осложнений, описываемых Я. В. Волколаковым, можно избежать.
В. И. Попов и В. И. Филин создали загрудинный канал под контролем зрения у одного больного и отрицательно отзываются о продольной стернотомии.
Б. А. Петров, который произвел самое большое количество операций загрудинной пластики в нашей стране, почему-то до сих пор выполняет загрудинный ход вслепую. Значит, те осложнения, о которых предупреждает Я. В. Волколаков, не так уж часто встречаются, если не побудили Б. А. Петрова прибегнуть к продольной стернотомии при загрудинной эзофагопластике.
Описывая предфасциальную загрудинную пластику пищевода, В. И. Попов и В. И. Филин отмечают, что этот способ проведения трансплантата стал разрабатываться с 1954 г. в клиниках, руководимых А. Г. Савиных (Томск) и А. Н. Мачабели (Рига). Методику же создания загрудинно-пред фасциального канала приводят ту, которой пользовались в Риге: резекция мечевидного отростка и проведение «изогнутого шпателя с направителем, который проводится непосредственно за грудиной, между задней поверхностью грудины и отслоенной внут-ригрудной фасцией сзади». Между тем методика образования загрудинно-предфасциального канала, применяемая в клинике имени А. Г. Савиных, была опубликована в 1960 г. (В. С. Рогачева) и в 1962 г. в трудах XXVII Всесоюзного съезда хирургов (А Г. Савиных).
Приводим подробное описание операции загрудинно-предфасциалыюй пластики пищевода из тощей кишки, применяемой в нашей клинике после резекции пищевода при раке.
Производят срединный разрез от мечевидного отростка до пупка, послойно вскрывают брюшную полость. Тщательно осматривают печень, поддиафрагмальное пространство и малый сальник на предмет выявления метастазов рака. Всякий подозрительный узелок иссекают и отдают на гистологическое исследование. После этого приступают к мобилизации начальных отделов тощей кишки общеизвестным путем, изолированно перевязывая и пересекая 3—4 мезентериальных радиальных сосуда (артерии и вены). По окончании мобилизации тощую кишку в начальном отделе пересекают. Конец ее, идущий от двенадцатиперстной кишки,- ана-стомозируют в бок кишки на уровне дистального отдела освобожденной (мобилизованной) брыжейки. Соустье, чаще Т-образное, накладывают двухрядным непрерывным кетгутовым швом. Конец выделенной кишки временно ушивают однорядным непрерывным кетгутовым швом. Измеряют тесемкой длину кишки по брыжейке для установления достаточности ее для проведения на шею. Если конец кишки достигает вырезки грудины, операцию продолжают до конца. Острые углы дуг мезентериальных сосудов на выделенной брыжейке делают более тупыми, обязательно обшивают край брыжейки петлистым швом непрерывной кетгутовои нитью, о чем уже сообщалось при описании операции по методу Савиных. Далее в брыжейке поперечноободочной кишки и Н§. §айгосоПсит делают отверстия. Через них проводят мобилизованную тощую кишку. Края техосо1оп подшивают на уровне межкишечного анастомоза. Весь кишечник, включая и приготовленную тонкую кишку, погружают в брюшную полость. Нужно внимательно следить, чтобы не перекрутить выделенную кишку.
Ложкой Тренделенбурга прикрывают все внутренности, в верхний угол раны ставят малый шейный крючок — таким образом становится хорошо видимой диафрагма вблизи мечевидного отростка. На 2—3 см кзади от мечевидного отростка во фронтальном направлении надсекают диафрагму на протяжении 7—8 см. С помощью тупфера и ножниц оттесняют кзади клетчатку переднего средостения, а затем отслаивают от грудины внутригрудную фасцию, которая здесь представлена в виде тонкого фиброзного листка. Теперь расширить и углубить ход лучше всего с помощью 2—3 пальцев правой руки, вводимых загрудинно. Пальцы отчетливо ощущают, что, кроме надкостницы, на грудине нет никаких тканей. Увеличив ход на длину пальцев и на ширину до 7—8 см (рис. 66), между грудиной и внутри -грудной фасцией с помощью длинной изогнутой иглы вводят 100—150 мл 0,5% раствора новокаина. Раствор действует и как анестетик, и как фактор для гидравлической препаровки, т. е. несколько отодвигает внутри-грудную фасцию от грудины. Далее берут длинные ножницы из набора инструментов А. Г. Савиных. Их немного изогнутые концы направляют вверх, к грудине (рис. 67). Ножницы с сомкнутыми браншами постепенно проводят между внутригрудной фасцией и грудиной, причем все время небольшими движениями кзади отодвигают от грудины фасцию. Так довольно свободно достигают уровня вырезки грудины. Чтобы провести концы ножниц на шею, приходится применять некоторое усилие для преодоления сопротивления внутригрудной фасции и мышц шеи, прикрепленных к грудине. После того как конец ножниц начинает пальпироваться над вырезкой грудины, бранши ножниц несколько разводят и в таком виде их не спеша извлекают в брюшную полость. Снова проводят ножницы в сомкнутом виде, теперь уже по готовому ходу, совершенно свободно, до шеи, но обратно извлекают с более широко разведенными браншами (рис. 69). Выводя ножницы раскрытыми, мы постепенно расширяем загрудинный ход. Ширина раскрытия ножниц, а значит, и загрудинного канала зависит от толщины кишечной петли б брыжейкой. В загрудинно-предфасциальный канал $ вводят влажные салфетки.
Операцию продолжают на шее. Под местной инфиль-трационной анестезией делают разрез кожи вокруг' пищеводного свища, конец пищевода отсепаровывают на 3—4 см. Надсекают шейные мышцы, прикрепленные к грудино-ключичному сочленению слева и к вырезке грудины. Расширяют ход за грудину с помощью пальцев. Из брюшной полости через загрудинный ход до шеи (после извлечения салфеток) проводят ножницы, концами которых осторожно захватывают влажную марлевую тесемку и протягивают ее до брюшной раны.
Из брюшной полости извлекают приготовленную для пластики пищевода кишку, проверяют правильность ее положения по отношению к выделенной брыжейке (не допускать перекрутов!). Конец кишки фиксируют к концу тесемки 1—2 швами. Ассистент, потягивая за тесемку с шеи, начинает проводить кишку загрудинно. В это время хирург подает и направляет из брюшной полости трансплантат таким образом, чтобы кишечная петля не подвернулась под брыжейку (рис. 70). Конец кишки выводят на шею. Ерыжейка обычно ложится кзади и несколько влево или вправо, а кишечная петля — спереди. Проведение кишки совершается свободно и беспрепятственно. Избыточные петли кишки, ушедшие в загрудинно-предфасциальный ход, лучше переместить в брюшную полость (без натяжения брыжейки!) и зафиксировать в таком положении, подшив 1—2 швами кишку к краю рассеченной диафрагмы.
Хирурги делятся на две группы. Двое накладывают пищеводно-кишечное соустье в области шеи конец в конец. Если возможно натяжение анастомоза при наложении соустья конец в конец, то лучше анастомозировать конец пищевода в бок кишки, — таким образом трансплантат удлиняется на 3—4 см (ширина кишки).
Двое других хирургов послойно зашивают брюшную полость. Так одномоментно заканчивается типичная загрудинно-предфасциальная пластика пищевода.
Для иллюстрации приводим выписку из истории болезни.
Больная И., 44 лет, повторно поступила в клинику 3/1У 1957 г. 11/ХП 1955 г. ей была сделана резекция пищевода по методу Добромыслова — Торека. Общее состояние больной вполне удовлетворительное.
Метастазов в брюшной полости не обнаружено. Произведена мобилизация тощей кишки, пересечено 3 мезентериальных радиальных сосуда; длина кишки 34 см. Сделан ход за грудиной. На шее выделен пищеводный свищ. Загрудинно проведена тощая кишка. Наложен пищеводно-кишечный анастомоз конец в конец двухрядным швом.
Послеоперационный период без осложнений. На 7-й день разрешено глотать жидкости, на 9-е сутки — полужидкую пищу. Через 2 недели после операции больная стала питаться через рот любой пищей.
Проведено рентгенологическое исследование: шейный отдел пищевода анастомозирует с тонкой кишкой, проведенной загрудинно. Анастомоз, расположенный на уровне верхнего края рукоятки грудины, проходим беспрепятственно. Петля тонкой кишки, расположенная несколько вправо от срединной линии, имеет обычные поперечные складки слизистой оболочки, хорошо перистальтирует и проходима беспрепятственно на всем протяжении.
Больная живет и хорошо себя чувствует более 9 лет.
Когда после обычной мобилизации тощей кишки ее длины не хватает, чтобы вывести конец на шею без натяжения брыжейки, мы поступаем следующим образом. Натягивая корень брыжейки за дистальный участок мобилизованной кишки по направлению вверх (к голове), рассекаем на корне серозный покров в месте наибольшего его натяжения в поперечном направлении. После рассечения брюшины на корне брыжейки конец кишки можно поднять на 5—6 см выше, чем прежде. В большинстве случаев этого бывает достаточно, чтобы вывести кишку через загрудинно-предфасциальный ход до шеи. Метод мобилизации корня брыжейки по Б. А. Петрову и Г. Р. Хундадзе нам представляется более травматичным и мы его не применяем.
Приводим выписку из истории болезни больного, у которого удлинение кишечной петли было получено за счет рассечения серозной оболочки на корне брыжейки.
Больной А, 34 лет, поступил в клинику 20/11 1958 г., 8/1Н ему выполнена резекция пищевода по методу Добромыслова — Торека. Послеоперационный период протекал удовлетворительно. Больной настаивал на создании пищевода. Во время подготовки ко второй операции у больного развился фурункулез, из-за которого пластику пришлось отсрочить.
13 произведена операция: лапаротомия, осмотр брюшной полости. Метастазов ие обнаружено. Мобилизована тощая кишка, пересечено 4 мезентериальных радиальных сосуда, длина кишки только 26 см. Подсечена серозная оболочка на корне брыжейки. Теперь кишки хватало до вырезки грудины, конец ее можно было поднять на 6—7 см выше, чем до этого. Сделан ход за грудиной до шеи. Пищеводно-кишечный анастомоз наложен конец, в бок.
Через неделю после операции больному было разрешено глотать жидкости. На 10-й день появился небольшой свищ в области анастомоза, который через неделю закрылся самостоятельно.
11 произведено рентгенологическое исследование: пищевод над вырезкой грудины анастомозирует с петлей тонкой кишки, проведенной загрудинно. Анастомоз свободно проходим для жидкой и густой контрастной массы. Петля кишки заполнилась на всем протяжении, перистальтирует, умеренно расширена, имеет обычный рельеф слизистой оболочки.
13 больной выписан из клиники. Питался исключительно через рот. Умер через Г/г года после резекции пищевода.
В тех случаях, когда никакие способы удлинения кишки не помогают довести ее до шеи и когда длины кишки хватает, но конец ее имеет несколько синюшный цвет, приходится мобилизованную кишечдую петлю или оставлять в брюшной полости на Г/з—2 месяца, или, лучше, в подкожной клетчатке передней грудной стенки. По прошествии указанного срока предпринимается пластика пищевода. Если кишечная петля оставалась в брюшной полости, то ее выделяют из спаек и без особого риска натягивают; иногда удается дополнительно пересечь мезентериальный сосуд. Кишку, которая прежде внушала сомнение в смысле ее жизнеспособности при проведении на шею, сейчас можно провести совершенно спокойно, не опасаясь ее некроза. За Р/г—2 месяца в выделенной брыжейке развиваются коллатерали, и кровоснабжение кишки становится лучше, чем сразу после мобилизации.
Приводим выписку из истории болезни.
Больной Я., 54 лет, повторно поступил в клинику 10/1У 1956 г.; 20/ХП 1955 г. ему выполнена операция резекции пищевода по методу Добромыслова — Торека.
При повторном поступлении состояние больного удовлетворительное; 17/1У 1956 г. предпринята попытка сделать искусственный пищевод. Лапаротомия, осмотр брюшной полости. Метастазов не обнаружено. При мобилизации тощей кишки после пересечения 4 мезентериальных сосудов и подсечения серозной оболочки на корне брыжейки длина кишки была всего 25 см, причем конец кишечной петли в 8—9 см имел синюшный цвет. Кишечную петлю уложили в брюшной полости и на этом операцию закончили.
Послеоперациощшй период протекал без осложнений, больной был выписан.
В третий раз поступил 25/1Х 1956 г. Состояние вполне удовлетворительное; 2/Х 1956 г. произведена загрудинно-предфасциальная пластика пищевода. Мобилизованная ранее кишечная петля свобод-
но лежала в нижней половине брюшной полости, имелись спайки только между ее петлями. Спайки рассечены. Длина кишки 25 — 26 см. Около конца кишечной петли дополнительно пересечен один мезентериальный сосуд, ее длина стала 30—31 см. Теперь кишки хватало. Сделан загрудинный ход. Выделен пищеводный свищ в области шеи. Загрудинно помещена кишечная петля, в области шейной раны наложен пищеводно-кишечный анастомоз конец в конец, с некоторым натяжением. Метастазов в брюшной полости во время операции не обнаружено.
На 5-й день после операции у больного образовался свищ в области пищеводно-кишечного анастомоза. Приблизительно через 2 недели свищ самостоятельно закрылся, и больной стал принимать пищу через рот.
29 проведено рентгенологическое исследование: пищевод в шейном отделе анастомозирован с тонкой кишкой, проведенной загрудинно. Проходимость пищеводно-кишечного анастомоза беспрепятственная. Тонкая кишка заполнилась свободно на большом протяжении, хорошо перистальтирует. Рельеф слизистой оболочки не изменен.
14 в хорошем состоянии больной выписан из клиники. Живет и хорошо себя чувствует более 10 лет после операции.
Примером того, как способствует удлинению кишки ее помещение в подкожной клетчатке передней грудной стенки, может быть следующее наблюдение.
Больной А., 62 лет, поступил повторно в клинику 26/111 1963 г.; 23/Х1 1962 г. ему была выполнена резекция пищевода и кардии методом Савиных (без одномоментной пластики) по поводу рака нижней трети пищевода. За год до поступления в клинику перенес инфаркт миокарда. При повторном поступлении состояние больного удовлетворительное.
10/1У 1963 г. предпринята попытка сделать искусственный пищевод. Лапаротомия, осмотр брюшной полости. Метастазов не обнаружено. При мобилизации тощей кишки можно было пересечь только-2-мезентериальных радиальных сосуда. После подсечения серозной оболочки на корне брыжейки длина кишки 25 см; конец кишки в 6—7 см приобрел синюшную окраску. Кишечную петлю поместили в подкожной клетчатке над грудиной. Конец кишки не достигал вырезки грудины на 4—5 см. На другой день при ревизии кишки ее конец в 5—6 см пришлось резецировать как нежизнеспособный и создать кишечный свищ. Послеоперационный период дальше протекал без осложнений.
Через 67 дней произведена загрудинно-предфасциальная эзофагопластика. Кишечная петля выделена из подкожной клетчатки и брюшной полости до межкишечного анастомоза. Ее длина 27— 28 см. Приготовленный трансплантат помещен в загрудинно-пред-фасциальный ход, конец кишки со значительным натяжением выведен из-за вырезки грудины. В области шеи наложен пищеводно-кишечный анастомоз. Послеоперационный период без осложнений.
4 произведено рентгенологическое исследование: пищевод над вырезкой грудины анастомозирован с тонкой кишкой, проведенной загрудинно. Проходимость анастомоза и искусственного пищевода беспрепятственная.
15/УН 1963 г. больной выписан из клиники. Прожил после резекции пищевода 2/г года и умер от метастазов рака.
Загрудинно-предфасциальная пластика после резекции пищевода выполнена у 56 больных: у 38 после резекции пищевода по методу Добромыслова — Торека (у одной больной прежде была сделана пластика пищевода, позднее резекция), у 17 — после резекции пищевода по методу Савиных, у 1 больного — после резекции верхнегрудного отдела пищевода с шеи (через верхнюю медиастинотомию). Все больные поправились; искусственный пищевод их вполне удовлетворял.
При создании загрудинно-предфасциалыюго канала плевротомия произошла у 5 больных (4 правосторонних и 1 левосторонняя). Ранение плевральных листков наблюдалось в первые годы работы, когда хирурги, по-видимому, недостаточно внимательно относились к отслойке внутригрудной фасции. У 51 больного загрудинно-предфасциальный ход сделан без нарушения целости плевральных листков.
Из 56 больных одномоментно пластика пищевода закончена у 39. Средний срок после резекции пищевода, через который была выполнена пластика, составил около 3,7 месяца (от 19 дней до 9 месяцев). У 17 больных искусственный пищевод был создан в два этапа, из них 5 больным, оперированным по методу Савиных, кишечная петля была заготовлена во время первой операции, но не проведена. На данную группу из 17 больных средний срок, через который была закончена пластика пищевода, составил 7 месяцев (от Р/2 до 12 месяцев).
Пищеводно-кишечный анастомоз зажил первичным натяжением у 37 больных, а у 19 в области пищеводнокишечного соустья на шее образовались свищи, возникавшие в различные сроки после операции, причем у 6 человек были точечные свищи, пропускавшие только воздух и закрывшиеся в течение недели. У 4 человек через свищ просачивалась только жидкость, истечение которой прекратилось самостоятельно в течение 1—2 недель. Более значительные свищи имелись у 9 человек, но и у них заживление произошло в сроки от 17 дней до 2 месяцев. Отмечено, что чем позднее образуется свищ, тем он меньше и закрывается быстрее. Свищи чаще возникали у тех больных, у которых наблюдалось натяжение в области пищеводно-кишечного анастомоза.
Может возникнуть вопрос, почему после резекции пищевода у больных раком искусственный пищевод (тощая кишка) помещается не антеторакально, что считается менее опасным, а загрудинмо?
Руководитель клиники А. Г. Савиных был всегда сторонником внутригрудного помещения искусственного пищевода. Для загрудинного проведения требуется меньшей длины кишечная петля, чем для предгрудинного. По нашим наблюдениям, средняя длина кишки, проводимой загрудинной, была 30—32 см. Мобилизация меньшего участка кишки таит в себе меньше возможностей получить некроз трансплантата. На 56 операций эзофагопластики некроза кишки, даже частичного, мы не наблюдали.
Приведенные данные о загрудинно-предфасциальной пластике пищевода после его резекции, по нашему мнению, довольно убедительно показывают, что этот путь проведения трансплантата нисколько не опаснее, чем предгрудинный. Тощая кишка как пластический материал для искусственного пищевода не должна уступать своего первенства толстой кишке.
В этом отношении совсем не убедительно высказывание В. И. Попова и В. И. Филина (1965) о том, что «ввиду частого омертвения тонкокишечного трансплантата следует ограничивать показания к внутригрудной тотальной эзофагопластике». Опыт указанных авторов по тонкокишечной пластике пищевода после операции Терека основан на 7 операциях, причем антеторакальных.
В. И. Попов и В. И. Филин пропагандируют толстокишечную пластику при непроходимости пищевода. Они выполнили эзофагопластику из толстой кишки у 140 больных, давшую 5,5% летальности. Наблюдалось большое количество осложнений: частичный некроз трансплантата — у 7 больных, непроходимость искусственного пищевода — у 7, непроходимость кишечника — у 9, перитонит—у 2, пептическая язва — у 2, причем из 140 оперированных больных только у 30 сделан загрудинный искусственный пищевод.
Опыт клиники имени А. Г. Савиных к концу 1965 г. составил 151 операцию загрудинной и загрудинно-предфасциальной пластики пищевода после резекции при раке и при рубцовой стриктуре. У 148 больных загрудинно помещена тонкая кишка и только у 3 — толстая. Послеоперационная смертность составила 3,3%. Из 5 умерших ни один не погиб от некроза трансплантата. Такое осложнение, как непроходимость искусственного пищевода, встретилось только у 1 больного. Непроходимость кишечника, пептическая язва, перитонит не наблюдались.
Сравнение наших данных с результатами В. И. Попова и В. И. Филина свидетельствует о том, что тонкокишечная загрудинная эзофагопластика не сложнее и не опаснее, чем антеторакальная и толстокишечная, и показания к ней ограничивать не следует.