Остановимся подробнее на осложнениях, которые наблюдаются у наших больных. После резекции пищевода по методу Савиных они значительно отличаются от наблюдавшихся после операции по Добромыслову—Тореку. Поэтому мы рассмотрим их отдельно.
Осложнения после резекции пищевода по методу Савиных. Эти осложнения наблюдались у 23 из 66 больных.
1 больных из пяти было второе осложнение — начало некроза кишки (искусственного пищевода).
2 больного было и второе осложнение — небольшой свищ в области пищеводно-кишечного анастомоза на шее.
Как видно из табл. 10, на 23 больных приходится 26 осложнений. Наиболее тяжелым осложнением, возникшим во время операции, был двусторонний пневмоторакс. Трое из 5 больных, у которых имелся двусторонний пневмоторакс, умерли в течение 1—2-х суток после операции. У двух из них тяжелое состояние усугублялось начинающимся некрозом тощей кишки, помещенной в заднем средостении. Трое умерших от указанного осложнения были оперированы в годы, когда пищеводная хирургия только начала применяться в клинике. Ранение второй медиастинальной плевры у них произошло спонтанно и не было замечено; 2 больных оперированы позднее. Повреждение плевр хирург видел, поэтому операцию закончил только резекцией пищевода без одномоментной пластики, причем у одного — под интубационным наркозом. После операции был аспирирован воздух из обеих плевральных полостей. Послеоперационный период протекал у этих больных гладко.
Грозным послеоперационным осложнением, приведшим всех 4 больных к смерти, был некроз тощей кишки— задне-медиастинального искусственного пищевода. Больные умерли на 2-й, 9-й, 20-й и 32-й день после операции. У больных, умерших на 9-й и 32-й день, через 3 суток после операции некротизированная кишка была извлечена из средостения и резецирована, однако развился гнойный медиастинит. У больного, умершего на 20-й день после операции, был некроз не всей мобилизованной тощей кишки, а верхнего ее участка величиной 10—12 см. Через неделю развился гнойный медиастинит и правосторонний гнойный плеврит. У больной, умершей через день после операции, имелся обширный некроз не только всей мобилизованной петли тонкого кишечника, но и значительного участка дистальнее выделенного.
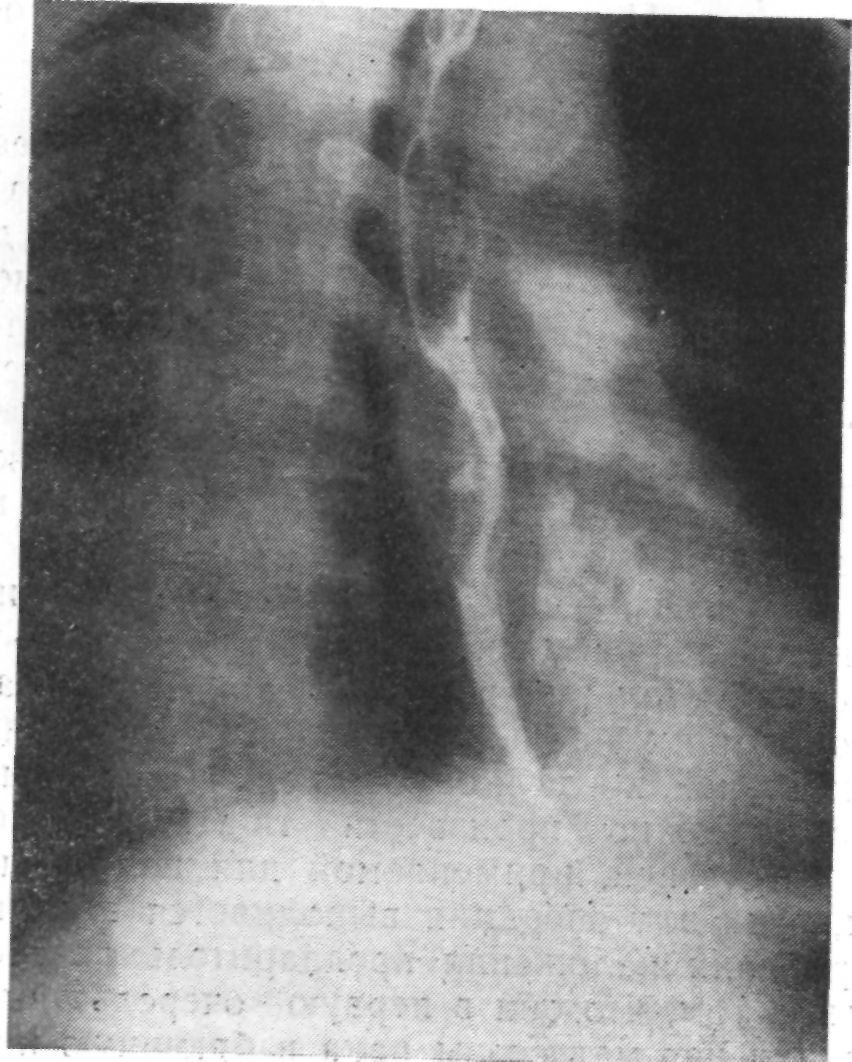
Следующим осложнением, которое привело к летальному исходу, было расхождение меж-кишечного анастомоза, возникшее на 9-й день после операции. Сразу же была предпринята повторная операция, но развились тяжелый шок, перитонит, интоксикация. В тот же день больной умер.
Приводим выписку из его истории болезни.
Больной Ю., 59 лет, поступил в клинику 22/111 1952 г. Клинический диагноз: рак нижне-грудного отдела пищевода, стадия II.
21/1У произведена резекция пищевода по методу Савиных с одномоментной тонкокишечной пластикой пищевода. Вначале послеоперационный период протекал без осложнений. На 4-е сутки больному разрешено было глотать воду, морс, на 8-е сутки — есть полужидкую пищу. В это же время больной начал ходить; 30/1У, на 9-е сутки после операции, утром были сняты швы в области шеи и передней брюшной стенки — заживление первичным натяжением. Днем у больного внезапно появились резкие боли в животе, состояние шока. Через час произведена операция: релапаротомия, во время которой было обнаружено расхождение меж-кишечного анастомоза. Анастомоз восстановлен. В брюшную полость введены тампоны. К вечеру 30/1У больной умер.
Острое расширение желудка развилось на о-й день после операции у одной больной. Поэтому через неделю после основной операции ей был наложен желудочный свищ. В дальнейшем возник разлитой фибринозный перитонит, и на 87-й день после операции больная умерла.
Приводим выписку из истории болезни.
Больная Б., 51 года, поступила в клинику 28/1У 1954 г. Клинический диагноз: рак нижне-грудного отдела пищевода, стадия II.
14/У произведена резекция пищевода по методу Савиных с одномоментной тонкокишечной пластикой пищевода. Гастростомию не делали.
В течение первых 4 дней после операции состояние удовлетворительное. На 4-й день больной разрешено глотать жидкости; проходимость искусственного пищевода хорошая. На 5-й день у больной стало нарастать вздутие живота, особенно в верхних отделах. Применявшиеся очистительные клизмы мало способствовали улучшению состояния; 20/У состояние больной значительно ухудшилось: живот вздут, особенно в левой половине, при пальпации его отмечается болезненность. 21/У состояние еще хуже: появились сильные боли в животе, особенно вздута и напряжена левая половина. Язык сухой, жажда. Ночью с 21 на 22/У больная срочно оперирована. При релапаротомии обнаружен резко вздутый желудок, переполненный жидкостью. После вскрытия желудка из него удалено около 3 л мутного, с примесью желчи, содержимого со зловонным запахом. Наложена гастростома.
После повторной операции состояние больной несколько улучшилось. Однако нормальной эвакуации из желудка добиться не удавалось. Пища, принимаемая через искусственный пищевод, частично попадала в желудок и там застаивалась. Было нагноение и частичное расхождение раны вокруг гастростомы. Состояние больной периодически становилось лучше; она сидела, пыталась ходить по палате; временами ей было хуже, пропадал аппетит, усиливалась слабость.
9/У1Н на 87-й день после резекции пищевода больная умерла.
Из патологоанатомического эпикриза следует, что в послеоперационном периоде возникло осложнение — атония желудка и острое его расширение. Произведена повторная лапаротомия и гастро-стомия, но после второй операции возникло частичное расплавление передней стенки желудка. Содержимое его попало в брюшную полость, развился разлитой фибринозный перитонит, который и явился непосредственной причиной смерти больной.
С этого времени в клинике каждому больному после резекции пищевода стали накладывать желудочный свищ.
Подобное осложнение — атонию желудка после резекции пищевода — описал в 1954 г. РхзсЬег. Его больная умерла на 5-е сутки после операции. Также сделал вывод, что после резекции пищевода с закрытием кардии следует накладывать желудочную фистулу.
Позднее появились работы Е. В. Лоскутовой, изучавшей секреторную и эвакуаторную функции желудка после резекции пищевода. Она нашла, что «после внутри-грудных резекций пищевода по Добромыслову—Тореку, сопровождающихся резекцией блуждающих нервов, наступает значительное нарушение в секреторной и эваку-аторной функциях желудка».
В результате послеоперационного осложнения, обозначенного патологоанатомами как послеоперационная асфиксия, умер один больной, у которого была опухоль верхнегрудного отдела пищевода. Операция прошла вполне удовлетворительно. Па 2-й и 3-й день после операции у больного периодически стали возникать приступы удушья, заключавшиеся ь затрудненном напряженном коротком вдохе и шумном продолжительном выдохе. Появлялся цианоз. Применялись всевозможные средства борьбы с удушьем, вплоть до трахеостомии, искусственного дыхания, однако на 4-е сутки после операции во время приступа больной умер.
Приводим выписку из истории болезни.
Больной М., 58 лет, поступил в клинику 15/ХН 1955 г. Клинический диагноз: рак верхне-грудного отдела пищевода, стадия II —III.
27/ХП произведена резекция пищевода по методу Савиных с одномоментной пластикой пищевода. Опухоль срослась с правой медиастинальной плеврой. Участок плеврального листка иссечен и остался на опухоли. Наступил правосторонний пневмоторакс. Однако операция протекала вполне удовлетворительно и была благополучно закончена.
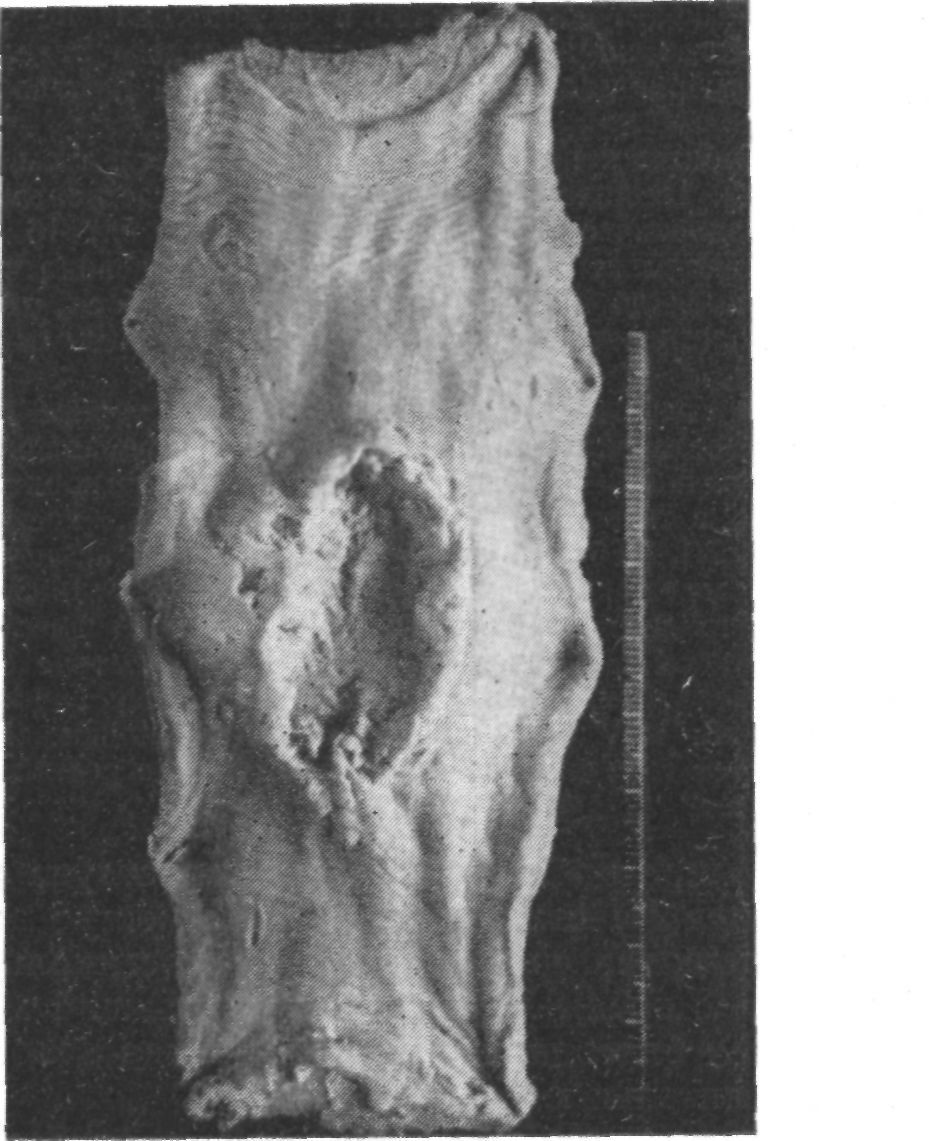
На следующий день после операции состояние больного удовлетворительное. Температура нормальная, пульс 96 в минуту, частота дыханий 24 в минуту, дыхание свободное. Артериальное давление 110/72 мм рт. ст. Голос хрипловатый (несколько травмирован левый возвратный нерв).
29/ХП состояние больного ухудшилось. Температура утром 37,7°, пульс 100 в минуту. Днем после банок больной стал задыхаться, появился страх удушья. Пульс около 150 в минуту. Некоторый цианоз кожи лица, пальцев рук. Больному давали кислород. Постепенно дыхание выравнялось. Ночь прошла спокойно.
30/ХП утром температура 36,9°, пульс 100 в минуту, дыхание свободнее, чем накануне. Лицо багрово-красного цвета. Голос шепотный. Больной говорил, что чувствует себя хорошо. В 13 часов 30 минут приступ затрудненного дыхания, цианоз. Дан кислород. Внутривенно введено 20 мл 40% раствора глюкозы, 1 мл (20 единиц) конвазида и 0,8 мл 0,1% атропина под кожу. Примерно через полчаса дыхание выравнялось. В 14 часов 30 минут снова приступ удушья: короткий затрудненный вдох и длинный шумный выдох. Постепенно дыхание прекратилось. Сознание отсутствовало. Цианоз кожи нарастал. Пульс оставался хорошим. В 15 часов 05 минут произведена трахеостомия. Из просвета трахеи аспирировано слизисто-кровянистое содержимое в небольшом количестве. Продолжали искусственное дыхание, давали кислород. Через 15—20 минут больной начал дышать самостоятельно. В 16 часов вернулось сознание. Пульс 96 в минуту, артериальное давление 115/70 мм рт. ст. Ночь прошла хорошо.
31/ХП в 7 часов 35 минут снова возник приступ удушья: шумное и затрудненное дыхание. Пульс 90—94 в минуту. Дан для вдыхания кислород, внутривенно введен 40% раствор глюкозы и 10% хлористый кальций. Затруднение дыхания нарастало. Проводилось искусственное дыхание. Появилась тахикардия. Больной стал вести себя беспокойно. В 9 часов 30 минут при явлениях асфиксии наступила смерть.
Результаты патологоанатомического вскрытия: состояние после операции резекции пищевода и пластики по методу Савиных. Двусторонний (небольшой!) пневмоторакс, кровоизлияния в область сосудисто-нервных пучков шеи. Рефлекторная асфиксия. Эмфизема клетчатки переднего средостения. Причина смерти: послеоперационная асфиксия.
Мы склонны были объяснить такое расстройство дыхания травмой и раздражением блуждающих нервов во время операции выделения высоко расположенной опухоли.
У остальных больных осложнения не были смертельными. У 8 человек в области пищеводно-кишечного анастомоза на шее возникли свищи, которые закрылись самостоятельно в различные сроки в пределах до 3 недель. Расхождение швов передней брюшной стенки на 10-й и 13-й день после операции наблюдалось у 2 больных. У обоих имелись небольшие гематомы в подкожной клетчатке области шва; кроме того, был легкий кашель. Разошлись кожные швы и швы апоневроза. В тот же день были наложены вторичные швы. У 65-летнего больного на 16-й день после операции появился ограниченный тромбофлебит левой голени, в вену которой во время операции вливали капельным методом кровь. Было предпринято соответствующее лечение и через неделю все явления стихли.
Наконец, последним осложнением, с каким нам пришлось встретиться, явился парез участка мобилизованной и оставленной в брюшной полости тощей кишки. У больного после резекции пищевода по методу Савиных и мобилизации начальных отделов тощей кишки для пластики пищевода к концу операции было обнаружено, что участок приготовленной петли длиной 8—10 см имел синюшный цвет. Было решено оставить ее в брюшной
полости. На 4—5-й день после операции отмечены вздутие живота и боли. Пришлось сделать лапаротомию. Конец кишки в 10—12 см был слегка цианотичен, отечен, а весь остальной участок мобилизованной кишки был раздут газами и не перистальтировал. Содержимое кишечной петли через прокол стенки было выпущено, появилась перистальтика, цианоз конца ее не определялся. Учитывая, что такая несколько воспаленная петля даст много спаек в брюшной полости, мы ее поместили подкожно на передней грудной стенке. В дальнейшем больному была выполнена загрудинно-предфасциальная пластика пищевода с использованием этой кишки.
Из 23 больных, у которых наблюдались осложнения, в послеоперационном периоде умерло 10. Самыми частыми, тяжелыми и смертельными осложнениями были некроз кишки — искусственного пищевода — и двусторонний пневмоторакс. С 1955 г., когда операция Савиных при раке пищевода стала применяться по разработанным показаниям, двусторонний пневмоторакс возник лишь 2 раза на 41 операцию. Значит, если резекцию пищевода по методу Савиных применять строго по показаниям, тяжелого осложнения в виде двустороннего пневмоторакса можно избежать.
Осложнения в виде некроза тощей кишки — искусственного пищевода — тоже можно устранить. После мобилизации кишечной петли, проводя ее в заднем средостении, не допускать подвертывания петель под брыжейку и даже малейшего натяжения ее. При выведении конца кишечной петли в шейную рану не следует торопиться с наложением анастомоза, а нужно выждать 10—15 минут, наблюдая за цветом конца трансплантата. При малейшем подозрении на неполноценность кровоснабжения кишечной петли (цианоз!) следует вернуть ее в брюшную полость и оставить там. Через 11/2—2 месяца эту кишку можно будет свободно, без опасности некроза, вывести через загрудинно-предфасциальный ход на шею и анастомозировать там с пищеводом (в области свища).
Нам представляется, что хирурги, которые с успехом пользуются для пластики пищевода толстой кишкой, имеющей лучшее кровоснабжение, чем тонкая, после резекции пищевода по методу Савиных могут проводить в заднем средостении толстую кишку и не бояться некроза. Значит, и второе смертельное осложнение можно преодолеть. Остальные Осложнения, приведшие к печальному исходу, были единичными.
Расхождение меж-кишечного анастомоза должно настораживать в отношении соблюдения режима питания больных раком через 7—10 дней после операции.
После того как мы стали заканчивать операцию наложением гастростомы, а в послеоперационном периоде следить за состоянием желудка, ни разу не наблюдалось острого расширения желудка, хотя застойные явления и бывали.
Смертельный исход в результате послеоперационной асфиксии еще раз подчеркивает, что локализация опухоли в верхне-грудном отделе пищевода является наиболее сложной для хирургического лечения. Останавливаться на остальных, не смертельных, осложнениях мы не будем. Укажем лишь, что их тоже нередко можно предупредить.
Как видно из табл. 11, единственным осложнением, которое повело к летальным исходам, было кровотечение
У одного из этих больных был еще и отек легкого.
У одной больной во время операции резецированы участки обеих медиастинальных плевр, был двусторонний пневмоторакс.
У одного больного резецированы участки обеих медиастинальных плевр, возник двусторонний пневмоторакс.
У одного больного опухоль располагалась в верхне- и средне-грудном отделах пищевода. Секционный диагноз: послеоперационное кровотечение в заднее средостение и полость правой плевры. Частичный ателектаз правого легкого. Отек левого легкого. На секции не было обнаружено отдельного, достаточно крупного, кровоточившего сосуда. Можно полагать, что выделение высоко расположенной опухоли пищевода, прилегавшей к дуге аорты, было достаточно травматично, что в дальнейшем, помимо кровотечения из артерий пищевода, рефлекторно повело к отеку легкого.
У второго больного, умершего от кровотечения, имелась обширная опухоль средне- и нижне-грудного отделов пищевода протяженностью 10 см. Опухоль с большим трудом высекалась из средостения. Секционный диагноз: массивное острое кровотечение в заднее средостение из артериального сосуда, метастазы рака в забрюшинные лимфатические узлы. У данного больного или не была перевязана одна из артерий пищевода, или с нее соскочила лигатура.
Осложнения у остальных больных (21) не были смертельными.
Серозный плеврит справа, наблюдавшийся у 6 больных, через 10—14 дней после соответствующей терапии был ликвидирован.
Пневмония (у 3 больных правосторонняя и у 2—левосторонняя) под влиянием лечения быстро купировалась и не оказала значительного влияния на состояние больных.
Сердечная слабость наблюдалась у 2 больных. Она наступила во вторую послеоперационную ночь и проявилась частым малым пульсом, общей слабостью, бледностью, холодным потом. Дежурный медицинский персонал применил сердечно-сосудистые средства: строфантин с глюкозой, камфарное масло, кофеин. Для вдыхания был дан кислород. К утру все явления прошли.
Верхний медиастинит, установленный при рентгенологическом исследовании в виде расширенной вправо тени, сопровождавшийся повышенной температурой тела, был у 2 больных. В течение 10 дней вводили антибиотики, и постепенно все явления стихли.
Хилоторакс наблюдался у 2 больных, у которых во время операции резекции пищевода при выделении опухоли был ранен грудной проток. Несмотря на то что оба конца протока были обшиты и перевязаны, в дальнейшем развился лихоторакс. У одного больного хилезная жидкость отделялась через дренажную трубку в небольшом количестве, и через месяц свищ в правой плевральной полости закрылся. У второго хилезная жидкость по дренажной трубке не поступала, трубку пришлось убрать. Лишь через 2 недели впервые путем пункции правой плевральной полости удалось получить хилезную жидкость. С этого времени при пункции через каждые 2—3 дня удалялось по 1—1,5 л инфицированной жидкости. Неоднократно переливали кровь, применяли противовоспалительное и общеукрепляющее лечение. Спустя 1‘/2 месяца после операции правая плевральная полость была дренирована. Больной выписан через 4 месяца после резекции пищевода с функционирующим плевральным свищом. Дома плевральный свищ закрылся, и больной поступил в клинику повторно для эзофагопластики.
Фурункулез развился у одного больного при общем хорошем состоянии. Введение пенициллина и переливание крови способствовали быстрому прекращению инфекции.
Нарушение эвакуации из желудка, выразившееся в жалобах на тошноту, тяжесть в подложечной области и вздутие желудка, было у одного больного. Ему в течение недели ежедневно по нескольку раз приходилось открывать желудочный свищ, выпускать содержимое и промывать желудок теплой водой. Постепенно эвакуация из желудка восстановилась.
У одного больного по окончании операции был обнаружен парез левого лицевого нерва, на другой день — левосторонний гемипарез. Консультант-невропатолог поставил диагноз сосудистого криза в районе правой средней артерии мозга по типу тромбоза. Проводилось соответствующее лечение. Через 24 дня после операции больному было разрешено сесть, через 34 дня — ходить. Явления пареза прошли почти полностью. Через Р/г месяца после операции больной был выписан из клиники в удовлетворительном состоянии.
Мы отнесли к осложнениям и обнаруженный в послеоперационном периоде парез правой руки у одного больного. Заключение невропатолога: множественные метастазы в головной мозг. Больной после операции поправился, но парез правой руки не прошел. Считаем, что из-за трудностей диагностики метастазов в головной мозг, которые до операции ничем не проявлялись, мы допустили ошибку, отнеся данного больного в группу операбельных.
Осложнения после других операций на пищеводе. Из 9 больных, которым были выполнены другие операции по поводу рака пищевода, осложнения наблюдались у двух. У одной больной, страдавшей раком нижне-грудного отдела пищевода, после диафрагмокруро-томии внеплеврально была выполнена резекция нижнего отдела пищевода с наложением пищеводно-желудочного анастомоза на 7—8 см выше уровня диафрагмы. На 9-й день больная умерла вследствие недостаточности анастомоза.
Второму больному с опухолью средне-грудного отдела пищевода III стадии и второй с опухолью в субкардиальном отделе желудка комбинированным подходом (правосторонняя торакотомия, лапаротомия и диафрагмотомия) была выполнена резекция грудного отдела пищевода и верхней половины желудка с наложением пищеводного и желудочного свищей. В послеоперационном периоде состояние больного было тяжелым, а на 7-ю ночь после операции возникла острая сердечно-сосудистая недостаточность. Вводили строфантин с глюкозой 2 раза в день, эуфиллин с глюкозой, камфарное масло, давали кислород. Только на 18-й день больному разрешено было сидеть в постели, на 25-й день ходить. Выписан из клиники на 36-й день после операции.
У остальных 7 больных осложнений в послеоперационном периоде не наблюдалось.
В общей сложности из 130 больных после резекции пищевода осложнения наблюдались у 48 (37%). Всего осложнений было 52, так как у 4 человек было по два послеоперационных осложнения. У 13 больных осложнения привели к смерти.
Ю, Е. Березов (1956) из 27 оперированных больных наблюдал осложнения у 20; всего осложнений было 38.
С. В. Гейнац и В. П. Клещевникова (1957) в результате осложнений в послеоперационном периоде потеряли половину своих больных. Н. А. Амосов (1958) наблюдал осложнения у 25 из 32 оперированных; 14 из них умерли.
К. Б. Крымова и соавторы (1962) из 42 радикально оперированных по поводу рака пищевода осложнения наблюдали у 27 человек с 20 летальными исходами.
Если сравнить характер послеоперационных осложнений, наблюдавшихся нами, и осложнений, описанных другими хирургами, то видна значительная разница. У наших больных наиболее частыми и тяжелыми осложнениями, влекущими за собой смерть, были некроз кишки — искусственного пищевода, двусторонний пневмоторакс и кровотечение в средостение. Тяжелыми, нередко смертельными, осложнениями, описанными другими хирургами, были сердечно-сосудистые и легочные расстройства, а также недостаточность пищеводно-желудочного анастомоза.
Одни хирурги (Е. Л. Березов, А. А. Писаревский) главные причины, ведущие к тяжелым послеоперационным осложнениям, видели во вскрытии второй плевральной полости, возникновении плевропульмонального шока и отека легких, что часто вело к смерти больных.
Другие авторы (Ю. Е. Березов, Н. М. Амосов, Н. М. Степанов, Н. И. Володько, с соавторами и др.) наиболее тяжелыми осложнениями, ведущими к летальному исходу, считают нарушение деятельности сердечнососудистой системы и органов дыхания.
Большинство же хирургов наиболее опасными осложнениями, ведущими часто к смерти больных, считают сердечно-сосудистую недостаточность, нарушение деятельности органов дыхания и недостаточность анастомоза.
Иногда расстройства сердечно-сосудистой системы и недостаточность функции органов дыхания в послеоперационном периоде объединяют в одно понятие сердечно-легочной недостаточности. Такое название указанных расстройств можно считать правильным, так как нарушение сердечно-сосудистой деятельности всегда вызывает недостаточность дыхания и, наоборот, расстройство функции дыхания приводит к глубоким изменениям деятельности сердца. Только в одних случаях ведущей, наиболее выраженной является дыхательная недостаточность, в других— сердечно-сосудистая. Поэтому в литературе их часто разделяют.
В настоящее время все хирурги знают, что чем травматичнее, длительнее протекает операция в плевральной полости, особенно при ранении второй медиастинальной плевры, тем больше будет выражена сердечно-легочная недостаточность в послеоперационном периоде.
Для борьбы с сердечнососудистой недостаточностью, возникающей в первые дни после операции, в настоящее время применяется весь арсенал сердечных и сосудистых средств. Нередко удается справиться с этим тяжелым осложнением.
Борьба с дыхательной недостаточностью, зависящей от скопления слизи в трахее и бронхах, заключается в отсасывании содержимого дыхательных путей. Для этого пользуются катетером, проведенным через нос в трахею, или выполняют эту манипуляцию с помощью бронхоскопии. Улучшение бывает кратковременным. Поэтому в последние годы для борьбы с дыхательной недостаточностью накладывают трахеостому, через которую удобно удалять из трахеи слизь и давать больным кислород. В случае необходимости можно применить искусственное дыхание с помощью специальной трахеотомической канюли и спиропульсатора. Хирурги, использовавшие трахеостомию при дыхательной недостаточности, считают эту операцию спасительной (И. К. Иванов, М. С. Григорьев и А. Л. Избинский, В. И. Казанский, П. А. Куприянов и соавторы, Б. Н. Аксенов, СоШз и др.).
Другими причинами, ведущими к дыхательной недостаточности, являются ателектаз и отек легкого, а также пневмония. Ателектаз пытаются предупредить расправлением легкого в конце операции перед зашиванием грудной стенки и тщательным удалением воздуха из плевральной полости сразу после операции и в ближайшие послеоперационные дни. Меры предупреждения и борьбы с отеком легкого недостаточно эффективны. Это осложнение почти всегда оканчивается смертельно.
Воспалительные явления со стороны легких предупреждаются с первых дней путем поворачивания больных в постели, дыхательной гимнастикой, введением антибиотиков, камфарного масла. Возникшее в послеоперационном периоде воспаление легких лечат, как обычную пневмонию.
Остановимся на следующем часто встречающемся, нередко смертельным, осложнении — недостаточности анастомоза. Работ, посвященных регенерации в области пищеводно-желудочного или пищеводно-кишечного анастомоза, изучению причин возникновения недостаточности, диагностике и лечению свищей в области соустья, исследованию лучших методов наложения соустий, имеется достаточно.
Л. Н. Гусева провела морфологическое исследование пищеводно-желудочного и пищеводно-кишечного анастомозов после резекции рака пищевода и кардии. Она установила, что на препаратах «с несостоятельностью соустья во всех случаях определяется краевой некроз анастомозированных органов с расстройством кровообращения этой области и последующим прорезыванием швов... Нетщательная адаптация слизистых области анастомоза ведет к проникновению инфекции в глубоко лежащие ткани, что может способствовать массивному разрастанию соединительной ткани, ведущей к сужению последнего». Исследования этого автора показали, что в течение 4 суток после операции в области анастомоза наблюдается отек, суживающий просвет соустья. Поэтому Л. Н. Гусева считает, что прием пищи раньше 6-го дня после операции «противопоказан и может способствовать расхождению краев анастомоза». Ее исследования интересны и ценны. О них следует помнить, выполняя операции на пищеводе, А. Г. Савиных придавал большое значение правильному сопоставлению слоев сшиваемых органов, особенно слизистых, оперированию без натяжения органов и без применения жомов. Он писал: «...физиологические приемы оперирования снижают травму, уменьшают процессы воспаления, предупреждают образование патологических рефлексов. Все это приближает к нормальной регенерации тканей в области всего операционного поля, что неизменно ведет к клиническому успеху».
Вопросу регенерации тканей в области анастомоза посвящены работы А. А. Ольшанского и И. Д. Кирпатовского. Т. Н. Михайлова на большом клиническом материале показала, что недостаточность швов соустья не является абсолютно смертельным осложнением. Она разработала меры профилактики недостаточности анастомоза, заключающиеся в сохранении «кровоснабжения пищевода, недопущении натяжения сшиваемых органов, пересечении пищевода на достаточном расстоянии от границ опухоли».
Б. Е. Петерсон провел большую экспериментальную работу по наложению пищеводно-желудочного и пищеводно-кишечного анастомозов разнообразными методами и при различных подходах. Результаты своих экспериментальных исследований он подкрепил клиническими наблюдениями и пришел к выводу, что чем проще наложен анастомоз, тем реже наблюдается его недостаточность. Анастомоз лучше накладывать «двухрядными узловыми швами», «в условиях хорошего доступа», «при щадящей кровообращение технике выделения пищевода».
Указанные работы были посвящены в основном изучению анастомозов, наложенных после резекции рака кардии. При выполнении операций по поводу рака грудного отдела пищевода принцип наложения анастомоза с тщательным сопоставлением слизистых, без натяжения линии анастомоза и с сохранением васкуляризации сшиваемых органов, остается. Однако появляется опасность некроза широко мобилизованного и высоко поднятого в грудную полость желудка. Для предупреждения некроза желудка при его мобилизации С. В. Гейнац предложил сохранять левую желудочную артерию, а А. А. Русанов разработал методику мобилизации желудка вместе с селезенкой.
Для лучшего сшивания пищевода и желудка с целью профилактики недостаточности соустья А. М. Бирюков разработал свой способ наложения пищеводно-желудочного анастомоза при раскрытой культе желудка. На 22 такие операции он не наблюдал недостаточности анастомоза.
Для укрепления линии анастомоза С. В. Гейнац подшивал медиастинальную плевру, Ю. Е. Березов укрывал всю линию анастомоза «желудочной или кишечной стенкой, иногда с дополнительным укрытием сальником, плеврой или брюшиной». При мобилизации желудка оставляют на большой кривизне кусочек сальника или желудочно-селезеночной связки и ими укрепляют анастомоз.
Б. В. Петровский предложил прикрывать анастомоз лоскутом из диафрагмы. М. И. Соколов применил этот метод в клинике, а А. Г. Черных в эксперименте доказал хорошее приживление лоскута диафрагмы в области анастомоза.
Для укрепления соустья рекомендуют в нижней трети пищевода прикрывать его большим сальником или серозно-мышечным лоскутом диафрагмы, в средней трети — куском париетальной плевры.
Проведены экспериментальные работы по применению перикардиальных пересадок с тромбофибриногеновым сгустком при операциях на пищеводе и по использованию плевры и перикарда для пластической хирургии пищевода.
Большое внимание хирургов и экспериментаторов к пищеводно-желудочному соустью говорит о том, что этот анастомоз в хирургическом отношении несовершенен, так как часто возникает недостаточность швов.
Так, по данным И. П. Такеллы, из 14 умерших после резекции пищевода у 7 имелась недостаточность анастомоза, по Г. К. Ткаченко, из 24 умерших у 8 причиной смерти было расхождение соустья. Такие же данные представил Б. А. Королев. Из 24 больных 9 умерли от просачивания анастомоза. Сообщил, что у его больных почти в 50% смерть наступила в результате недостаточности швов соустья.
В. И. Казанский с соавторами писал: «Улучшение непосредственных результатов при раке пищевода и кардии с переходом на пищевод должно идти по пути устранения основного послеоперационного осложнения — недостаточности пищеводно-желудочного или пищеводно-кишечного анастомоза. По-видимому, на данном этапе развитии хирургии пищевода это осложнение является основной причиной послеоперационных неудач».
В 1957 г. Б. В. Петровский сообщил, что, по его данным, летальность от расхождения анастомоза с 65% снизилась до 25%- Это хорошее достижение, но все же причиной смерти каждого четвертого больного является указанное осложнение. Ю. Е. Березов и М. С. Григорьев, изучив послеоперационную летальность, приведенную в литературе, и собственные данные, отмечают, что почти *Д умерших погибает от недостаточности швов анастомоза. По данным, собранным из 11 центров, на 259 смертельных осложнений после резекции пищевода отметили 76 случаев недостаточности соустья (29,3%).
По поводу операции при раке кардии писал, что настоящую причину расхождения анастомоза следует искать не в механически-технических факторах, а в функциональных расстройствах, общих нарушениях в организме больного раком и местных функциональных изменениях желудка и пищевода.
Можно согласиться, что общие нарушения в организме больного раком значительно отражаются на заживлении анастомоза. Это неоднократно наблюдали хирурги в своей практике. Иногда технически хуже наложенный пищеводно-кишечный или пищеводно-желудочный анастомоз у больного с доброкачественной стриктурой пищевода заживал без образования свища, в то время как безупречный в техническом отношении анастомоз у канкрозного больного того же возраста осложнялся недостаточностью.
Что касается местных функциональных расстройств пищевода и желудка, то бесспорно одно. Широкая мобилизация желудка на большом протяжении с дополнительным пересечением нервов и сосудов более опасна вследствие возможности расхождения швов анастомоза с пищеводом в грудной полости, чем в случаях сохранения основных сосудистых стволов. Не напрасно, которому принадлежит самое большое количество наблюдений по резекции пищевода при раке, проводит желудок подкожно, накладывает анастомоз с пищеводом на шее, где недостаточность анастомоза не является смертельным осложнением. Не случайно и то, что наши
отечественные специалисты по пищеводной хирургии (Б. В. Петровский, В. И. Казанский, В. И. Попов и В. И. Филин, А. А. Русанов, А. А. Вишневский, Ю. Е. Березов и др.), испытав различные методы операций, в последние годы при раке грудного отдела пищевода стали применять операцию Добромыслова — Торека, отказавшись от высоких одномоментных анастомозов в грудной полости.
К довольно частым осложнениям относится и расширение желудка, находящегося в грудной полости. Оно возникает из-за пареза его после пересечения блуждающих нервов. Расширенный желудок оказывает отрицательное влияние на сердечную и дыхательную деятельность. Кроме того, он способствует натяжению анастомоза, что может привести к возникновению недостаточности швов соустья.
С целью уменьшить расширение желудка в грудной полости С. В. Гейнац (цит. по М. С. Григорьеву и Б. Е. Аксенову) предложил проводить рифление его стенок с помощью швов. Другим методом улучшения эвакуации из «грудного желудка» является пилоромиотомия (С. В. Гейнац и В. П. Клещевникова, Бе Вакеу, Соо1еу, Г)ип1ор, и др.).
Во время операции вводят в желудок через нос так называемый зонд Левина, через который аспирируют содержимое желудка в течение нескольких дней. В последние годы стали применять двойной полихлорвиниловый зонд, с помощью одной трубки которого удаляют содержимое желудка, а через вторую трубку, расположенную в кишке, со 2-го дня начинают вводить питательные жидкости. Применение указанных мероприятий позволило успешно бороться с нарушением эвакуации «грудного желудка».
Мы описали осложнения, наиболее часто встречающиеся в послеоперационном периоде. Имеется много других, более редких осложнений, которые иногда трудно предвидеть, а значит и предупредить.
К редким осложнениям относятся инфаркт миокарда, эмболия сосудов мозга, профузное кровотечение из культи желудка, кровотечение через свищ между аортой и желудочно-пищеводным анастомозом, диафрагмальная грыжа, острый некроз поджелудочной железы, недостаточность коры надпочечников и многие другие. Большинство из них ведет к неблагоприятному исходу.
Нельзя не отметить, что ранее редко встречавшееся осложнение —тромбоэмболия легочной артерии —в последние 5—Ш лет стало наблюдаться чаще. Так, от этого осложнения погиб один из 13 умерших после операции больных у В. И. Казанского с соавторами; у М. С. Григорьева оно послужило причиной смерти у 10 из 106 умерших (9,4%).
Первым критерием полезности предпринимаемого хирургического вмешательства является число выживших непосредственно после операции больных.
Представлены далеко не все статистики, опубликованные в литературе, так как у части авторов неблагоприятные исходы даны совместно после резекции при раке кардиального отдела желудка и при раке пищевода, или вместе со смертельными исходами после пробных и паллиативных операций.
Наша цель была по возможности представить данные, касающиеся послеоперационных исходов после резекции пищевода по поводу рака его грудного отдела.
Как видно из табл. 12 и 13, по данным отечественных и зарубежных хирургов, летальность на большое количество операций в среднем составляет 35—31,1%, т. е. каждый третий больной после операции умирает.
Однако заметны сдвиги в сторону уменьшения послеоперационной летальности. Если в 1953 г. Ои1§етапп представил сборные данные о 700 операциях с 41,4% неблагоприятных исходов, а в 1957 г. Кехапо сообщил о 714 операциях с 44,5% летальности, то за несколько последних лет при увеличении количества операций и числа оперирующих хирургов (что особенно надо учесть) летальность снизилась на 8—10%. Данные В. И. Попова и Ыакауата показывают, что число неблагоприятных исходов можно значительно снизить. Изучая работы приведенных хирургов, можно понять, что своими успехами они обязаны методам операций, которыми пользуются для резекции пищевода.
В. И. Попов и В. И. Филин применяют преимущественно двухэтапные операции: сначала делают резекцию пищевода по Добромыслову—Тореку, потом эзофагопластику.
Ыакауата сам признает, что успех зависит от применяемого им метода операции с антеторакально проведенным желудком и анастомозом в области шеи. Такая методика дала у него наименьшую смертность: 8,5% на 271 оперированного больного.
Наивысшая летальность (С. В. Гейнац и В. П. Кле-щевникова, Н. М. Амосов, М. С. Григорьев и Б. Н. Аксенов, Б. А. Королев) была получена после одномоментных операций типа Гарлока и комбинированных типа Льюиса.
Мы никоим образом не хотим умалять значения ранней диагностики локализации опухоли в пищеводе, предоперационной подготовки, метода обезболивания, квалификации и опыта хирурга в течении послеоперационного периода и исходе операции. Однако приведенные данные отчетливо показывают, что результат операции в немалой степени зависит и от ее методики. По нашему мнению, относительно низкая летальность (10%) после резекции пищевода в нашей клинике в значительной мере зависит от применяемых методов операции.
Рассмотрим исходы наших операций (резекции пищевода) в зависимости от локализации опухоли (табл. 14). При опухолях, расположенных в верхне-грудном отделе пищевода, возникло наибольшее количество осложнений и почти 7з оперированных не перенесли операцию. Эти результаты полностью подтверждают данные литературы о редкости резекции пищевода при раке высокой локализации, о большом количестве послеоперационных осложнений и неблагоприятных исходов.
При локализации опухоли в средне-грудном отделе мы получили вполне удовлетворительные непосредственные исходы после резекции пищевода: из 76 оперированных умерло трое (4%).
Однако при резекции по поводу опухоли нижне-грудного отдела пищевода летальность у нас достигает 17,8%.
Чем же объяснить такое значительное несоответствие установившейся в хирургии пищевода закономерности?
В табл. 15 представлены количество резекций пищевода и исход при различных методах операций. При локализации опухоли в нижней трети пищевода из 8 больных, умерших после операции, 7 оперированы по методу Савиных. Однако эти цифры отнюдь не могут порочить метод. Следует учесть, что 6 человек из этого числа умерли до 1955 г. (в первый период), когда шла разработка операции и ее выполняли любому больному раком пищевода без соответствующих показаний. Из 6 больных у трех смерть наступила в результате двустороннего пневмоторакса.
Если исключить из числа 45 больных с локализацией опухоли в нижней трети пищевода 10 оперированных в первый период с 7 неблагоприятными исходами, то на 35 больных с указанной локализацией, оперированных с 1955 г. различными методами строго по установленным показаниям, мы потеряли после операции одного (2,9%). Таким образом, получается полное соответствие наших послеоперационных исходов, зависящих от локализации, результатам, полученным большинством хирургов.