К сожалению, как свидетельствуют данные литературы, только одному из 4 больных раком пищевода, обратившихся за хирургической помощью, удается выполнить резекцию пищевода.
Части остальных больных облегчить страдания могут так называемые паллиативные операции. К ним относятся применяемые в настоящее время гастростомия, обходные анастомозы, интубация ракового сужения пищевода пластическими трубками.
Гастростомия. Операция гастростомии по сравнению с другими паллиативными операциями при раке пищевода имеет самую длинную историю и пока наиболее распространена. Особенно часто наложение желудочного свища применялось в тот период, когда резекция пищевода при раке была редкой операцией и не давала удовлетворительных результатов. Тогда гастростомия была единственной операцией, облегчающей участь больных с полной непроходимостью пищевода. За 125 лет существования операции гастростомии было предложено несколько десятков методов наложения желудочного свища, различные модификации, но каждый из них имеет свои недостатки. Чаще всего применяются наиболее технически простые и дающие меньшее число осложнений методы Витцеля, Штамма — Кадера и Марведеля (Б. А. Петров, А. Д. Очкин, Е. Н. Петрова, Ю. Е. Березов, В. П. Зиневич и др.). Способ образования желудочного свища, предложенный отечественным хирургом Г. С Топровером, также не лишен недостатков и, по опыту Б. А. Петрова, М. П. Суетиной и Е. Н. Петровой, при раке пищевода его следует применять очень осторожно.
Мы для наложения гастростомы пользуемся в основном методом Штамма—Кадера.
Летальность после операций гастростомии при раке пищевода колеблется от 5,8%, до 40% (М. Р. Марцинович, Ю. Е. Березов) и даже 55%. Такая разница в количестве неблагоприятных исходов не связана с применяемым методом гастростомии или квалификацией хирурга, а определяется состоянием больного в то время, когда был наложен желудочный свищ.
Так, сообщая о 5,8% смертности после гастростомии, отмечает, что с введением в хирургическую практику операции резекции пищевода наложение желудочного свища производят все реже. Значит, большинство его больных было оперировано в тот период, когда гастростомия была единственной операцией, и свищ накладывался значительно раньше, чем это делается сейчас у неоперабельных и истощенных больных. Не приходится удивляться тому, что у Ю. Е. Березова из 174 больных, подвергшихся гастростомии, после операции умерло 70, так как у 13 больных имелись пищеводно-бронхиаль-ные свищи, а 27 были в таком тяжелом состоянии, что умерли от кахексии. Ю. Е. Березов сообщает, что операцию гастростомии он применял только у неоперабельных больных.
В 1932 г. М. Р. Марцинович ставил вопрос, что выгоднее: ранняя или поздняя операция, со свищом или без свища проживет больше больной. Он писал: «Не всегда больной с начинающимися явлениями затруднения в глотании согласится на такую операцию, как гастростомия. Только прогрессирование болезни и нарастающая угроза голодной смерти сломит его сопротивление». На основании своих наблюдений М. Р. Марцинович считал, что гастростому следует накладывать лишь тогда, когда больной начинает недоедать и ощущает голод, т. е. у ослабленных больных и, по-видимому, в большинстве своем уже неоперабельных. Вот почему у этого автора также была 40% послеоперационная летальность.
Всем хирургам известно, что чем раньше наложен желудочный свищ больному раком пищевода, тем лучше непосредственный исход.
В 1938 г. А. М. Заблудовский писал: «Больные раком пищевода, не могущие уже передвигаться самостоятельно, превратившиеся в постельных, не должны уже подвергаться гастростомии. Подлежат вмешательству лишь те больные, у которых истощение не достигло еще крайних пределов и которые ходят еще свободно».
Е. Н. Петрова, проанализировав 664 операции гастростомии за 2—3 десятка лет, отметила 18,2% смертности. Она установила, что по пятилетиям летальность колебалась от 5 до 29%- На основании своих исследований автор подчеркивает, что «следовало бы предпочесть раннюю гастростомию, как только распознан рак пищевода, так как в этот период операция проста, малоопасна и обещает замедлить течение болезни, устраняя раздражение опухоли пищей, проходящей по пищеводу», но, учитывая «отрицательные психические переживания больных», сотрудники клиники не спешат с операцией, «если жидкая пища свободно проходит».
В настоящее время, когда применяется операция резекции пищевода, вопрос о раннем наложении желудочного свища больным раком пищевода не ставится. Современные хирурги сходятся на том, что гастростому следует накладывать только в том случае, когда больному нельзя произвести резекцию пищевода из-за распространенности процесса или тяжести общего состояния (Ю. Е. Березов, В. П. Зиневич, Н. М. Амосов и др.).
В. И. Казанский в 1959 г. писал: «С онкологической точки зрения, наложение гастростомы, прекращающей питание через пищевод и тем самым постоянное раздражение пищей опухоли, значительно замедляет темп ее развития, а метастазирование возникает много позже, чем при других паллиативных операциях; срок жизни больных удлиняется».
Возможно, что срок жизни больных раком пищевода и удлиняется, если свищ наложен в начале заболевания, но не у тяжелых, истощенных неоперабельных больных. Наряду с этим совершенно очевидно, что при полной непроходимости пищевода желудочный свищ спасает больного от быстрой голодной смерти.
По данным литературы, невозможно определенно установить, что гастростомия способствует удлинению жизни больного раком пищевода. В. П. Зиневич, например, отмечает, что при раке верхне-грудного отдела пищевода гастростомия в состоянии Продлить Жизнь на 5,5 месяца. ДУПзоп с соавторами считают, что гастростомия не удлиняют жизни, а могут дать некоторое облегчение в последние дни жизни больного.
По данным, на 133 неоперабельных больных раком пищевода и кардии средний срок выживания с желудочным свищом был 2,4 месяца. По Ю. Е. Березову, на 31 больного с гастростомои средняя продолжительность жизни выписанных составила 6,9 месяца, умерших в клинике— 13,3 дня, наибольшая продолжительность жизни — 19 месяцев.
Данные нашей клиники по применению гастростомии у неоперабельных больных раком пищевода за описываемый период (1947—1965) следующие. Желудочный свищ как единственно возможный метод лечения был выполнен у 61 больного; 10 из них умерли в клинике (16,4%) и 51 больной был выписан. В клинике больные умерли в сроки от 2 до 66 дней после операции; средняя продолжительность их жизни была 25,3 дня; 4 больных умерли через 2, 5, 6 и 8 дней после операции от общего истощения, 6 —через 21, 24, 32, 44, 45 и 66 дней после наложения желудочного свища от основного заболевания, перфорации рака пищевода, пищеводно-трахеального свища и вызванных ими осложнений.
Таким образом, наши данные соответствуют литературным, по которым неоперабельные больные раком пищевода после гастростомии умирают часто в стационаре и основными причинами смерти являются общее истощение или сам раковый процесс.
Из 45 наших больных, которым гастростома была наложена после пробной операции, умерло 7 (15,5%), т. е. смертность примерно такая же, как и в предыдущей группе. Однако это не совсем так: 5 больных из 7 умерли от осложнений, связанных с пробными вмешательствами, шестой — от абсцесса левого легкого после пневмонии и седьмой — от основного процесса.
После всего сказанного возникает вопрос: если гастростома не спасает значительное число неоперабельных больных от быстро наступающей смерти (в стационаре) и очень сомнительно, способствует ли она продлению жизни выписавшихся больных, то стоит ли ее применять?
Ответ может быть один: для тех больных, которые с трудом глотают жидкости, а радикальная операция противопоказана из-за распространенности процесса или тяжелых сопутствующих заболеваний, а также для тех, кто резко истощен, ослаблен и не в состоянии перенести ка-кой-либо операции большого масштаба, единственной операцией, спасающей от голодной смерти, является гастростомия.
Мы совершенно согласны с Ю. Е. Березовым, что гастростомия «всегда должна существовать в арсенале хирурга как последнее средство».
Обходные анастомозы. Гастростомия имеет два основных недостатка: 1) оказывает неприятное психическое воздействие на больного и 2) больной нуждается в определенном уходе за свищом. Лучшими паллиативными операциями являются обходные анастомозы, пищеводно-желудочный и пищеводно-кишечный.
Обходной анастомоз, вернув больному возможность глотать любую пищу, вселяет в него веру в излечение.
Это основное преимущество обходных анастомозов перед гастростомией при неоперабельном (нерезектабельном) раке пищевода.
Обходные пищеводно-желудочные и пищеводно-кишечные анастомозы при неоперабельном раке кардии с переходом на пищевод впервые широко стали применяться в 40-х годах XX столетия проф. А. Г. Савиных (1939, 1940) при чрездиафрагмальном подходе к кардии и пищеводу. После того как несколько позднее получил распространение трансплевральный доступ к пищеводу и кардии, многие хирурги стали выполнять обходные анастомозы при неудалимых раковых опухолях кардии и нижнего отдела пищевода (В. И. Казанский, Б. В. Петровский, А. А. Полянцев, В. П. Зиневич, И. Я- Бойков и др.).
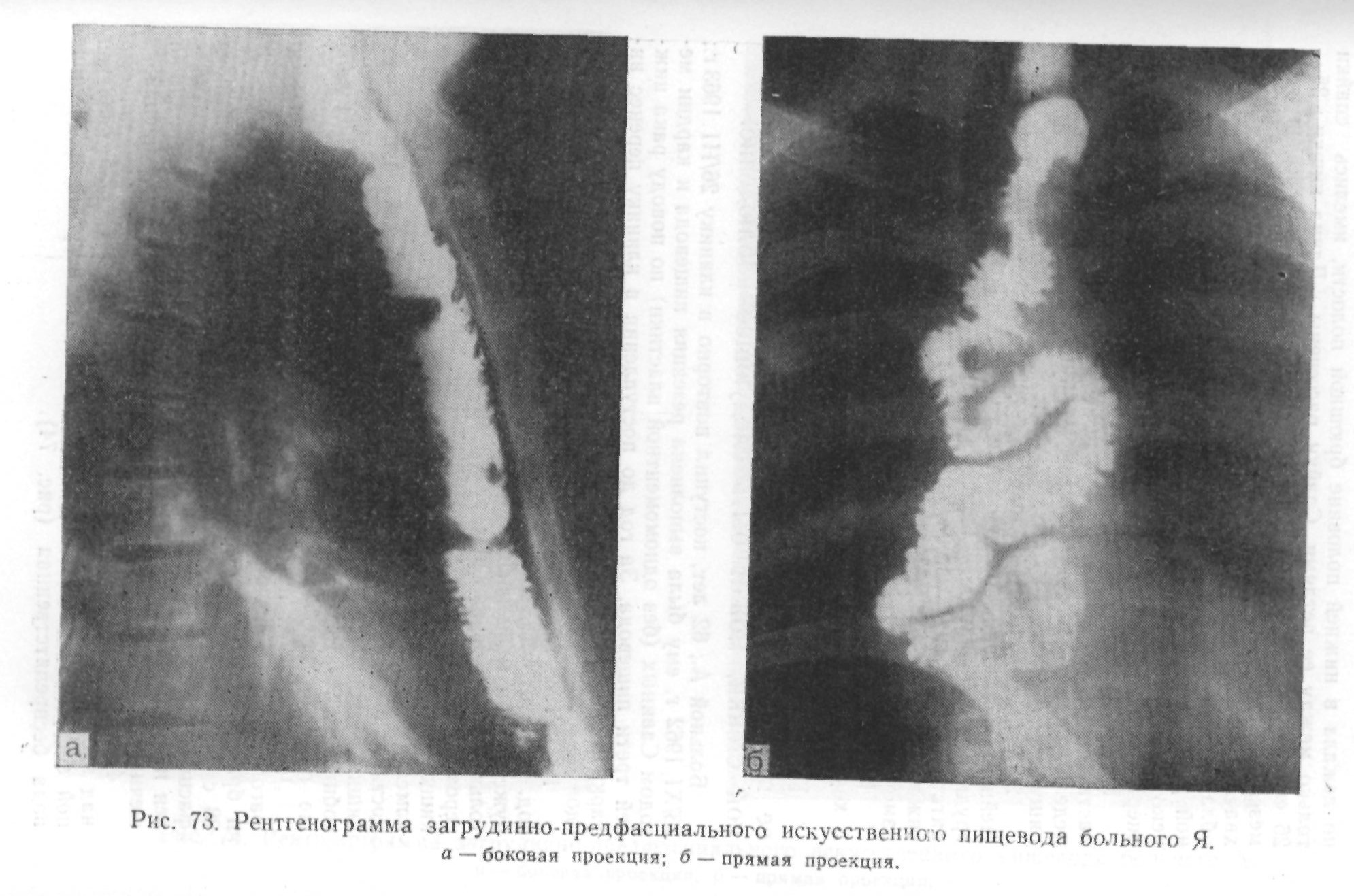
В. И. Казанский писал, что пищеводно-желудочный и пищеводно-кишечный анастомоз в обход опухоли «является идеалом паллиативных операций... Непосредственная удача этих операций, радостное настроение больных заставили нас принять за правило во всех случаях пробной торакотомии, когда установлена неудалимая опухоль, осуществлять обходной анастомоз. Это операция истинного милосердия и она должна заменить гастростомию, за которой останется место только для высоко расположенных опухолей пищевода».
Р. Т. Панченков на основании опыта 15 обходных операций при неоперабельном раке пищевода с 2 неблагоприятными исходами пришел к следующим выводам:
1) обходная операция пищеводно-желудочного и пище-водно-кишечного анастомоза... есть операция выбора;
2) ...желудочно-пищеводный анастомоз или кишечно-пищеводный анастомоз — идеал паллиативных операций при раке пищевода и кардиального отдела желудка.
B. П. Зиневич сообщил о 39 обходных анастомозах у неоперабельных больных раком кардии и нижнего отдела пищевода. Послеоперационная летальность составила 23% (9 человек). Автор указал, что «обходные анастомозы, снимая полностью дисфагию, в состоянии продлить жизнь больного на 1 месяц...» и что «большинство хирургов считает обходные анастомозы идеальными паллиативными операциями». Однако при раке средней трети пищевода в клинике, руководимой С. В. Гейнац, где работал В. П. Зиневич, обходные анастомозы не применялись.
Не у всех хирургов создалось такое хорошее впечатление от обходных анастомозов. Е. Л. Березов писал: «Эзофагогастро- или эзофагоеюностомии как обходные операции мы проводим чрезвычайно редко и не видим в них большого смысла, они все-таки достаточно сложны». Подобного мнения придерживается Н. М. Амосов. В 1956 г. Ю. Е. Березов сообщил, что число паллиативных обходных анастомозов постепенно уменьшается, так как они мало удлиняют жизнь, а операциями являются большими и сложными.
C. С. Юдин, подчеркивая, что он не имеет собственного опыта в наложении обходных анастомозов при неуда-лимом раке кардии и пищевода, очень сдержанно относился к этой операции. Он не разделял восторженного отношения Р. Т. Панченкова к обходным анастомозам.
С. С. Юдин писал: «И хотя, конечно, идея паллиативных обводных операций при неудалимых раковых опухолях кардии представляется сомнительной, тем не менее можно привести существенное соображение в оправдание таких вмешательств. Дело в том, что их проводят не с заранее обдуманным намерением, а вынужденно, т. е. если при чресплевральной эксплорации пищевода и желудка в последний момент выяснится, что радикальная операция неосуществима, а риск ее завершения был бы слишком велик и не оправдан, то вместо того, чтобы зашить грудную полость и диафрагму, не устранив непроходимости пищевода, действительно вполне целесообразно сделать высокое соустье пищевода и дна желудка».
Мы присоединяемся к мнению хирургов, считающих, что у тех больных, которым предпринимается пробная операция с надеждой на резекцию опухоли кардии и нижнего отдела пищевода, а в результате карцинома оказывается неудалимой, создание обходного анастомоза будет наилучшей паллиативной операцией.
Однако рак пищевода, о котором идет речь в данной работе, судя по статистическим данным, более чем в половине случаев локализуется в средней трети и лишь примерно в 25% в нижней трети пищевода. Кроме того, известно, что чем выше расположена опухоль, тем меньше надежды на ее удаление. Следовательно, в паллиативных операциях будут нуждаться главным образом больные с опухолью в средне-грудном и верхне-грудном отделах пищевода. Описанные выше обходные анастомозы при левостороннем торакальном подходе для больных с высокой локализацией опухоли пищевода неприменимы.
При неоперабельном раке грудного отдела пищевода в последние 10—15 лет используются обходные анастомозы типа искусственных пищеводов из тонкой или толстой кишки и из желудка, причем трансплантат помещается под кожей, загрудинно или в грудной полости. Реже применяются высокие внутригрудные анастомозы при комбинированном подходе по Льюису.
Н. И. Еремеев, описав операцию загрудинного искусственного пищевода, рекомендовали применять ее как паллиативную при неоперабельном раке пищевода.
У, сообщивших об операциях загрудинной пластики (в 5 случаях из тонкой кишки и в 1—из толстой), создалось хорошее впечатление об этом вмешательстве. Они писали: «В настоящее время мы обычно используем средостенный обход для всех больных в удовлетворительном состоянии со злокачественной обструкцией среднего или верхнего грудного отдела пищевода и для больных с не резецируемыми опухолями нижне-грудного или абдоминального пищевода». В дальнейшем они советовали у больных раком среднего или верхнего грудного отдела пищевода применять «кобальтовую» терапию или в благоприятных случаях предпринимать хирургическое лечение. Таким образом, во всех случаях рака среднего или верхнего грудного отдела пищевода предлагают выполнять сначала загрудинную пластику пищевода.
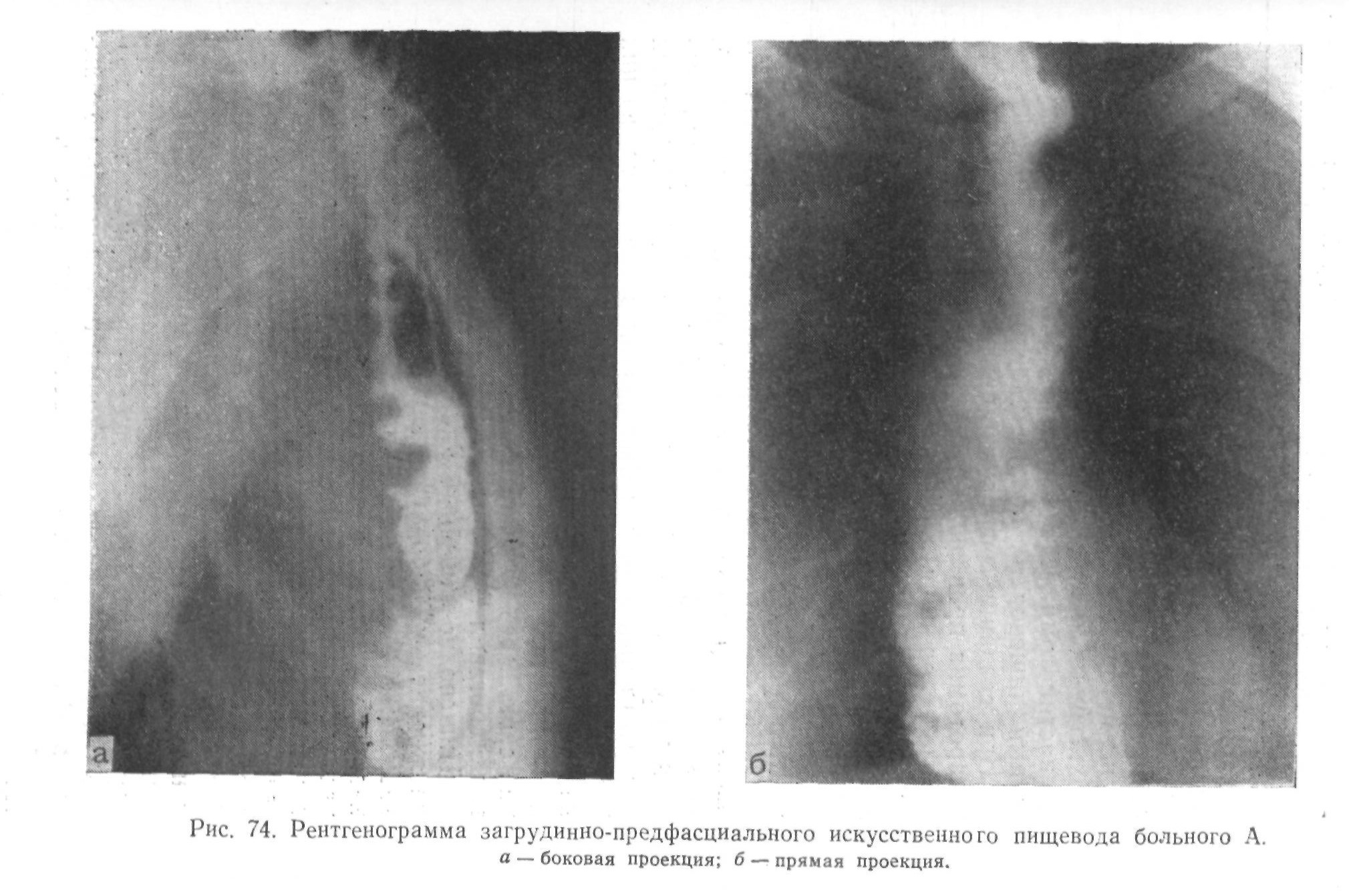
Подводя итог трехлетнего опыта хирургического лечения рака пищевода, пришли к заключению, что в случаях, когда распространенность процесса и состояние больного не дают надежды на длительное излечение, предпочтительнее ограничиться паллиативной операцией вместо резекции (имеется в виду обходной анастомоз), хотя они получили на 47 таких вмешательств при раке нижней трети пищевода 21% неблагоприятных исходов, а на 26 операций при раке средней трети — 50% смертельных исходов.
С соавторами сообщили о паллиативных анастомозах у 92 больных с 28% послеоперационной летальности.
В нашей стране обходные анастомозы при неоперабельном раке грудного отдела пищевода широко применяли Ю. Е. Березов и Е. В. Потемкина. В 1961 г. они сообщили о 41 операции обходного анастомоза; 17 больных умерли не выписываясь из стационара после операции, (41,5%). У более крепких больных, которым пытались удалить опухоль комбинированным методом по Льюису, выполнялись высокие внутригрудные анастомозы. У 28 тяжелобольных в качестве «операции отчаяния» авторы создали подкожный пищевод из участка толстой кишки (у 26) или тонкой кишки (у 2). Ю. Е. Березов и Е. В. Потемкина пишут: «Лучшее впечатление из типов обходных анастомозов у нас оставляет операция «отключения опухоли», заключающаяся в пересечении пищевода выше и ниже нерезектабельной опухоли, иссечении слизистой в оставляемом сегменте пищевода и формировании антеторакального искусственного пищевода за счет подкожно помещенного желудка. В имеющейся литературе мы не нашли описания подобной операции». Авторами выполнено шесть таких операций с двумя неблагоприятными исходами.
Они пересекали грудной отдел пищевода в двух местах на расстоянии 5—6 см, после чего сшивали дистальный и проксимальный концы пищевода или накладывали пищеводно-желудочный анастомоз, тем самым восстанавливая непрерывность. Высеченный участок пищевода оставался в средостении с зашитыми или незашитыми концами. Велись наблюдения за оставленным сегментом пищевода. С течением времени на месте участка пищевода образовалась киста, которая достигала определенных небольших размеров и в дальнейшем не увеличивалась. Тот факт, что кисты с течением времени не растут, авторы объясняют так: «Видимо, размер кисты само-ограничен, потому что по мере того, как давление в кисте увеличивается, секретирующие железы атрофируются и размер кисты остается стационарным». Предприняли свои опыты с той целью, чтобы при большой неоперабельной опухоли пищевода после ее отсечения с обеих сторон было удобнее и проще наложить обходной пищеводно-желудочный анастомоз в плевральной полости. Так они оперировали одного больного и получили хороший непосредственный исход.
У нас складывается впечатление, что операция подобна операции «отключения опухоли», описанной Ю. Е. Березовым и Е. В. Потемкиной, только первые авторы после пересечения пищевода вблизи опухоли анастомоз накладывали в грудной полости, а вторые — в области шеи, поместив желудок предгрудинно.
В последующих работах Ю. Е. Березов с соавторами и С. И. Юпатов проводили дальнейшее изучение больных с обходными анастомозами при неудалимых опухолях пищевода и кардии. В монографии Ю. Е. Березова и М. С. Григорьева приводится уже 47 операций обходных анастомозов при раке пищевода с 19 неблагоприятными исходами (40,4%), в том числе 8 операций «отключения опухоли».
Следует упомянуть об операциях. Он еще в 1951 г. сообщил о 28 операциях обходных анастомозов в виде искусственного пищевода из толстой кишки, помещенной под кожей или в переднем средостении у больных с неудалимой раковой опухолью пищевода. После операции умерло 6 человек; у 14 — были свищи на шее и только у 2 они закрылись самостоятельно; 10 больных со свищами умерли в течение 20 дней — 2'/2 месяцев. Из 28 больных лишь 6 выписались из стационара.
Исходы паллиативных обходных анастомозов при неоперабельном раке пищевода, опубликованные, малоутешительны. Наши данные мало отличаются от приведенных.
У 31 больного раком грудного отдела пищевода и у 4 больных раком кардиального отдела желудка и нижнего отдела пищевода с неудалимыми опухолями были выполнены обходные анастомозы в виде искусственного пищевода из тощей кишки. Из 35 больных, подвергшихся такой паллиативной операции, у 33 кишечная петля была помещена загрудинно (умерло в клинике 9 больных, или 27,3%) и у 2 — антеторакально (умер 1 больной). Таким образом, из 35 больных умерло 10, что составляет 28,5%.
Причиной смерти 7 больных явилось расхождение швов пищеводно-кишечного анастомоза на шее, повлекшее за собой медиастинит, а при подкожно расположенной тощей кишке — флегмону предгрудинной клетчатки; у 2 — некроз небольшого участка конца тощей кишки и медиастинит; 1 больной, у которого имелся свищ в области пищеводно-кишечного анастомоза на шее, умер через 54 дня после операции от основного процесса — рака среднего грудного отдела пищевода.
Из 25 больных, выписанных из клиники, у 13 не было осложнений в послеоперационном периоде; у остальных 12 имелись свищи в области анастомоза на шее, но все они закрылись самостоятельно в различные сроки. У большинства выписанных больных мы не отметили улучшения общего состояния после операции, хотя проходимость пищи по искусственному пищеводу была беспрепятственной.
Данные литературы и наши наблюдения, касающиеся обходных анастомозов при неоперабельном раке пищевода, свидетельствуют, что такие паллиативные операции дают высокую послеоперационную летальность и большое число осложнений; только небольшое число больных выписывается из стационара, чувствуя себя относительно здоровыми. В. К. Заславский определенно считает, что обходные анастомозы слишком сложны и в качестве паллиативных операций применяться не должны.
Что касается продления жизни больным с обходным анастомозом, то по этому поводу имеются различные сведения.
По например, у больных с нерезецируемыми опухолями и обходными анастомозами период выживания в среднем составляет 7,4 месяца. В. П. Зиневич сообщает, что обходные анастомозы могут продлить жизнь больного на 1 месяц. По данным И. Я .Бойкова, средняя продолжительность жизни после различных паллиативных операций при раке пищевода и кардии равна 5—6 месяцам. В литературе имеются лишь единичные сообщения о продолжительности жизни больных после обходных анастомозов до 1 года и больше (В. И. Казанский, одно наше наблюдение и др.).
Поэтому нельзя не согласиться со след) ющим высказыванием Н. М. Амосова: «Хотя в принципе возможно наложение пищеводно-желудочного и пищеводно-кишечного анастомоза, но практически это едва ли имеет смысл, поскольку сложная операция не оправдывается ее очень скромными результатами». В 1957 г. Б. В. Петровский писал: «Н. И. Еремеев предложил проводить тонкую кишку через переднее средостение и соединять ее с пищеводом на шее. По нашему мнению, при неоперабельном раке пищевода такая травматическая операция недопустима».
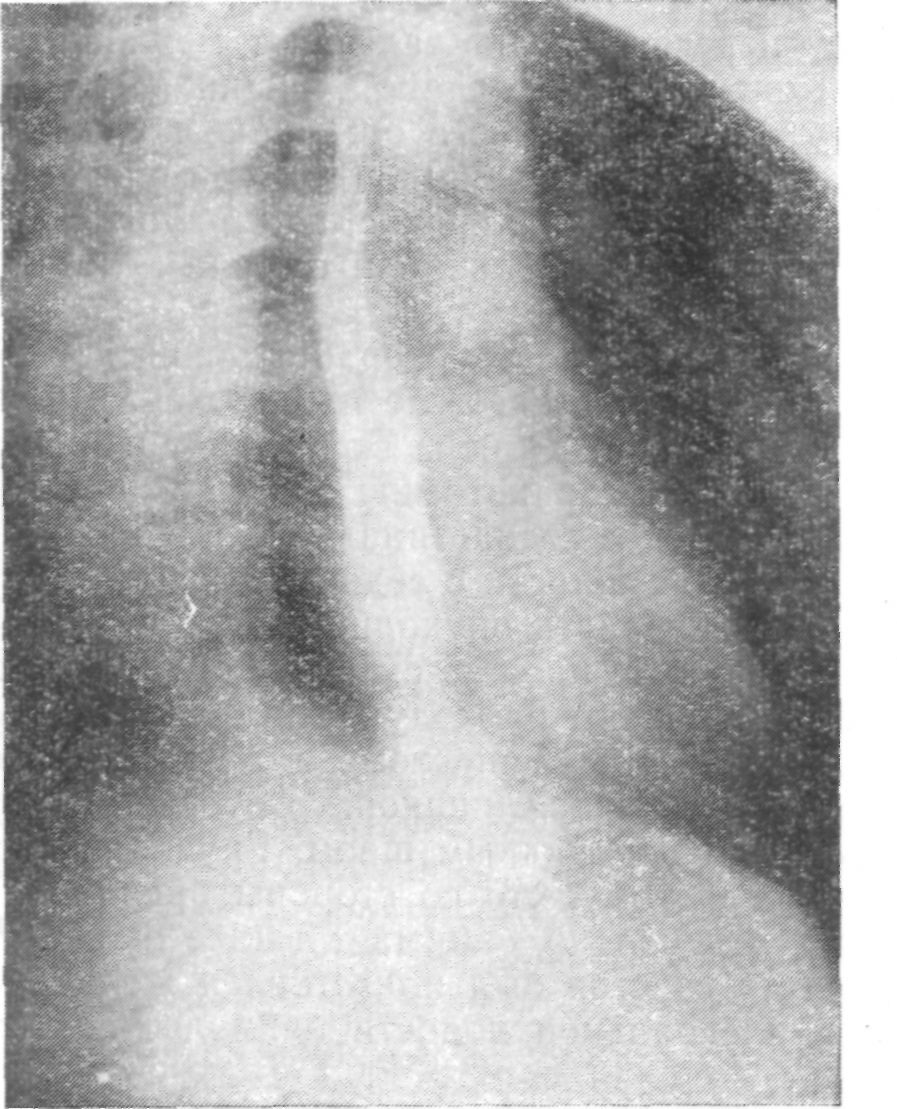
Наш опыт, охватывающий 35 операций создания искусственного пищевода при неудалимом раке и свидетельствующий о высокой летальности, особенно по сравнению с результатами 56 подобных вмешательств после резекции пищевода (ни одного летального исхода), послужил основанием тому, что в последние годы в клинике эта операция стала редкой. Неоперабельные больные плохо переносят эти довольно сложные вмешательства, у них возникает большое количество осложнений в послеоперационном периоде, которые часто приводят к смерти больных.
Мы считаем, что при неудалимой опухоли пищевода показания к операции обходного анастомоза следует ограничивать.
Интубация ракового сужения пищевода пластическими трубками. В 1927 г. была опубликована работа, предлагавшего проводить через суженный раковой опухолью участок пищевода с помощью эзофагоскопа воронкообразную серебряную трубку. Таким образом можно было восстановить проходимость пищевода. Однако трудность введения трубки при значительных сужениях пищевода и возможность перфорации, некрозы стенки пищевода в области опухоли привели к тому, что эта методика не получила распространения.
Более чем 20 лет спустя, убедившись во время операции в невозможности удалить опухоль пищевода, рассек стенку пищевода над карциномой и провел «через суживающую опухоль под прямым зрением» серебряную трубку. Затем было назначено рентгеновское облучение опухоли, давшее благоприятный результат. В 1954 г. сообщили о 19 случаях хирургической интубации у 18 больных раком пищевода. Во время «торакального исследования, когда выясняется, что опухоль нельзя экстирпировать», после рассечения стенки пищевода над опухолью авторы проводили через суженный карциномой просвет пищевода пластмассовую трубку и зашивали пищевод. Из 18 больных после операции умерло 6 (33%). Средний срок выживания был 3,4 месяца. Авторы писали: «Хирургическая интубация лучше другой паллиативной операции гастростомии или еюностомии тем, что ее можно выполнить во время первоначального торакального исследования и избежать лишней операции, а также тем, что такая интубация обусловливает хорошее самочувствие больного, позволяя ему глотать».
С применением пластмассовых трубок для интубации пищевода при раке за рубежом этот паллиативный метод получил достаточное распространение.
Сообщил о 103 операциях «перманентной интубации» за 9 лет (с января 1948 г. по январь 1957 г.). По его данным, «не было смертей, которые можно было бы приписать операционной процедуре, хотя некоторые осложнения встречались. Срок пребывания в госпитале был от 2 до 15 дней, в среднем 5 дней». Продолжительность жизни этих больных после выписки из стационара «варьировала от 3 недель до 2'/2 лет, средний срок выживания после введения протеза равнялся 8'/2 месяцам». Методика интубации была такая: по проводнику с помощью эзофагоскопа вводили полутвердую специально подобранную по размеру пластическую трубку с проксимальным флянцем (расширением). Даже при торакотомии трубку ставили с помощью эзофагоскопа, пищевод не рассекали. Место сужения обычно расширяли бужированием.
Авторы выполняли и другие паллиативные операции. Сравнивая различные методы, они установили следующее: «Когда показано паллиативное лечение, то техника интубации давала самые удовлетворительные результаты с минимальным числом осложнений и летальных исходов... Гастростомия в наших руках была совершенно неудовлетворительной в качестве паллиативного пособия».
Лучшей паллиативной операцией при раке пищевода также считает проведение пластических трубок через суженный отдел. По его мнению, введение пластических трубок во время торакотомии часто является опасным для жизни больного, а введение трубки через эзофагоскоп — трудным и травматичным. Поэтому предлагает две свои операции.
Первая операция применяется при раке верхнего и среднего грудного отделов пищевода. Делают разрез на шее слева, рассекают пищевод, вводят эзофагоскоп, бужируют опухоль и вставляют трубку Левина. После удаления эзофагоскопа по трубке Левина проводят пластическую трубку до упора воронкообразного расширения. Проксимальный конец трубки Левина проводят в рот и 4—6 дней трубка служит для кормления больного. Дефект в пищеводе зашивают.
Вторая операция применяется при раке нижне-грудного отдела пищевода и кардии. Производят лапаротомию, гастротомию, расширение просвета пищевода в области опухоли. Затем из желудка проводят трубку Левина до рта, где к ее концу подшивают пластическую трубку и низводят через опухоль до упора воронкообразного расширения. К нижнему концу пластической трубки из желудка фиксируют небольшую воронку из пластмассы, чтобы трубка не сместилась вверх. Автор считает, что предложенные им операции наименее травматичны и легко выполнимы.
В последние 3—4 года за рубежом опубликовано много работ, посвященных интубации пищевода, в которых авторы описывают свой опыт применения различных пластических трубок, вводимых через просвет пищевода разными методами.
В отечественной литературе первые сообщения о внутри-пищеводном протезировании пластическими трубками появились в 1958 г. И. А. Медведев и В. И. Францев писали о 15 своих операциях при неоперабельном раке пищевода и кардии. Трубку из полиэтилена или хлорвинила длиной от 5 до 12 см с диаметром 0,9 — 1,3см вводили через разрез стенки пищевода выше опухоли во время торакотомии. Авторы отметили, что «первый опыт применения паллиативной операции реканализации внутригрудного отдела пищевода пластическими трубками показал преимущество подобной операции перед гастростомией».
Г. Л. Ратнер предложил для интубации трубку — «бутон», которую можно проводить через суженный отдел пищевода не только в направлении сверху вниз, но и снизу вверх при раке кардиального отдела желудка и нижнего отдела пищевода, рассекая стенку желудка во время лапаротомии.
В. И. Казанский считает, что «эта операция хотя и восстанавливает проходимость пищевода, однако насильственная перфорация опухоли, постоянное раздражение ее трубкой ускоряет темпы развития опухоли и создают реальную угрозу ускорения процесса диссеми-нации рака. Поэтому это оперативное вмешательство при неоперабельных опухолях пищевода не встречает сочувствия среди онкологов».
С целью продлить жизнь неоперабельным больным Т. Т. Даурова, А. И. Рудерман и Т. П. Евстигнеева после интубации просвета пищевода пластмассовым протезом при раке стали проводить ротационную рентгенотерапию. Таким образом лечили 10 больных; продолжительность жизни у 7 была в среднем Н'/г месяцев.
Число работ, посвященных интубации или реканализации при неоперабельных опухолях пищевода, увеличивается (И.М.Бородин, А.А. Вишневский, А. У. Краснер, А. А. Шайн и др.). О самом большом количестве операций (100) сообщил В. К. Заславский. Он приводит новые предложения для безопасного введения трубок, методы их надежной фиксации в пищеводе, возможные осложнения.
Мы не имеем собственного опыта в применении пластических трубок с целью интубации у больных с неудалимыми опухолями пищевода. При изучении литературы по этому вопросу у нас сложилось определенное впечатление, что у ряда больных эта операция заслуживает внимания.
Подводя итог обсуждения паллиативных операций при раке пищевода, можно сказать следующее. Наиболее совершенной паллиативной операцией при неудалимои раковой опухоли пищевода является обходной пищевод-но-желудочный или пищеводно-кишечный анастомоз. Такой анастомоз с пересечением пищевода выше опухоли в целях отключения ее для избежания травматизации пищей не может вызвать возражений и со стороны онкологов.
Однако операция обходного анастомоза сложна и тяжела для ослабленного распространенным опухолевым процессом больного. Поэтому обходные анастомозы как паллиативные вмешательства могут применяться только у наиболее молодых и крепких больных.
В тех случаях, когда с надеждой выполнить резекцию пищевода производят торакотомию, но опухоль неудалима, а проходимость пищевода значительно нарушена, следует провести интубацию пищевода пластмассовой трубкой.
У неоперабельных и ослабленных больных с резко нарушенной проходимостью пищевода, которые не подлежат даже пробным операциям, следует накладывать желудочный свищ или вводить пластическую трубку в суженный отдел пищевода без операции.
Хирург, вынужденный ограничиться паллиативным вмешательством, прежде всего должен решить, какая из этих операций наиболее переносима для данного больного, и только после этого приступать к ее выполнению,
Заканчивая работу о хирургическом лечении больных раком пищевода, нельзя хотя бы вкратце не остановиться на широко применяемом для лечения карциномы пищевода лучевом методе.
Рак пищевода — плоскоклеточный рак, при котором воздействие лучей должно давать хороший эффект. Считают, что при раке верхних двух третей пищевода следует применять лучевое лечение. Наблюдения Кет и др. показывают, что рентгенотерапия при раке пищевода дает паллиативный эффект.
Применили рентгенотерапию у 56 больных. Из них 83% умерли в первый год, до 3 лет никто не дожил, средний срок жизни был 6,7 месяца, в то время как из радикально оперированных ими 9 больных один живет около 5 лет.
Применивший лучевове лечение у 399 больных раком пищевода, сообщил, что отдаленные результаты плохие: только двое прожили без рецидива 5 лет. Плохие результаты получил: из 296 больных раком пищевода у 55% лечение было прервано из-за повышенной температуры и лейкопении, 81% больных умерли к концу 1-го года, после 2 лет живы 3%.
Л. М. Гольдштейн, применявший метод долговременного дробного облучения через не смещаемую свинцовую решетку, отметил также, что лечение носило паллиативный характер; 75% больных умерли в течение 1-го года; ни один не пережил 5 лет (на 102 больных).
В нашей стране Я. Г. Диллон один из первых стал широко пользоваться лучевой терапией при раке пищевода. Он применил рентгеновское облучение со многих полей (30—40), концентрически расположенных вокруг очага, и получил хорошие непосредственные результаты. По данным Т. Г. Лариощенко и С. И. Алексеевой, использовавших методику Диллона у 58 больных, хороший паллиативный результат наблюдался у 28 и клиническое непосредственное излечение — у 15 (из них один жил 2’/г года и один — 4 года 8 месяцев).
С введением в практику рентгенотерапии ротационного метода облучения как непосредственные, так и отдаленью результаты лечения больных раком пищевода стали лучше.
Из 88 больных, леченных рентгеновыми лучами ротационным методом, 77 получили полный курс и у 50 из них не отмечалось признаков заболевания. Через 3 года были здоровы 8 больных, через 5 лет — 4, через 6 лет— 1 больной. Автор отмечает, что метод применялся у неоперабельных больных при любой локализации опухоли в пищеводе. Если облучать операбельных больных, результаты, возможно, были бы лучше.
Сообщил о результатах лучевого лечения 155 больных на вращающемся столе. Из них 2% больных были здоровы 5 лет, 4% —3 года; у 17% наступило улучшение, 4,5% умерли от метастазов, у 57%—изменения отсутствовали или отмечено ухудшение. У 17 больных было кровотечение, у 34 — перфорация пищевода. Считает, что по сравнению с облучением полями ротационное лечение немного лучше.
А. И. Рудерман приводит данные о 302 больных раком пищевода, подвергнутых ротационному облучению. Из 302 больных клиническое излечение наблюдалось у 37%, паллиативный эффект — у 39%. Из группы «клинически излеченных» жили более 2 лет 16% больных, более 4 лет — 7% и более 5 лет — 5 больных.
Для улучшения результатов лучевого лечения рака пищевода предложена сочетанная лучевая терапия (внутриполостное облучение пакетом радиоактивного кобальта и рентгенотерапия). Б. 3. Сухоруков, применив такой метод лечения, получил хороший результат: из 13 больных 4 живы И/г года.
Сообщили, что после смерти 2 больных раком пищевода через 17 и 34 месяца после комбинированного наружного и внутриполостного лечения во время секции в пищеводе не удалось обнаружить остаточную опухоль.
С 1958 г. в отечественной литературе появились первые сообщения о лечении больных раком пищевода радиоактивным кобальтом—телегамматерапии (Ш. М. Бейбутов). В настоящее время телегачиматерапия с помощью отечественной установки ГУТ-Со-400 применяется во многих рентгенорадиологических и онкологических учреждениях нашей страны. Проводится детальное изучение как непосредственных, так и отдаленных результатов лечения больных раком пищевода, исследуется влияние данного вида лучей на организм и т. д. Свидетельством повышенного интереса к телегамматерапии при раке пищевода является большое количество работ, посвященных этому вопросу.
Полученные авторами результаты довольно разноречивы и зависят от многих причин: 1) от стадии рака пищевода, 2) от методики облучения, 3) от общего состояния больного и др. Тем не менее М. А. Волкова и Г. А. Зедгенидзе совершенно определенно отмечают, что результаты телегамматерапии гораздо лучше, чем рентгенотерапии.
По данным 3. Ф. Лопатниковой, из 200 леченых больных 24% живут более 2 лет и 5% —свыше 5 лет. По Г. А. Зедгенидзе, из 214 больных, подвергшихся облучению с помощью установки ГУТ-Со-400, 117 жили более 2 лет (55%), 1 — 3/т года, 2 — около 7 лет. Это лучшие результаты, описанные в отечественной литературе по вопросам лучевого лечения рака пищевода. Следует отметить, что 3. Ф. Лопатникова, помимо наружного облучения, в некоторых случаях применяла и внутриполостной метод гамматерапии. Кроме того, она назначала и химиотерапевтические препараты «с целью повышения эффективности лечения».
Результаты, полученные И. А. Поповой, В. П. Шакировой и Л. И. Сергеевой, гораздо хуже. Несмотря на то что, по данным Л. И. Сергеевой, из 130 больных раком пищевода, находившихся под наблюдением, у 2 была I стадия заболевания, у 58 — II, у 41 —III и только у 29 — IV стадия, более 2 лет жили только 8 человек.
А. И. Рудерман, наблюдавший больных раком пищевода, облучавшихся радиоактивным Сз137 (цезий-137), установил, что непосредственное действие на опухоль гамма-излучения Сх11 , Со60 и рентгеновского излучения практически идентично.
Изучение влияния гамма-лучей на рак пищевода продолжается.
В литературе имеются данные о высоковольтной рентгенотерапии рака пищевода. Наблюдали 27 больных, получивших полный курс лечения; из них пять были клинически здоровыми 2, 10, 8, 3 и 2 года. В то же время 8ои1Ьшск и Со1е отметили, что облучение опухоли пищевода как стандартными рентгеновыми лучами, так и высоковольтными лучами с их большей глубинной дозой дало неудовлетворительные результаты.
Применив глубокое рентгеновское облучение у 12 больных, отметили, что 5 из них живут и здоровы, а 7 умерли. Среди умерших у 4 на вскрытии признаков карциномы не обнаружено. Авторы делают вывод, что рак пищевода можно излечить глубокой рентгенотерапией с направленным пучком.
Для лечения рака пищевода применили излучения бетатрона. Под их наблюдением было 56 больных, из них 47 закончили курс облучения (5500—6500 г). Больные хорошо переносили лечение, лучевой болезни не отмечено. Средний срок выживания больных был 10 месяцев; 4 живут 31, 29, 28 и 19 месяцев после окончания курса, у 8 больных наступила смерть от перфорации опухоли пищевода. На основании своих наблюдений авторы отмечают: «Не похоже на то, чтобы бетатронная терапия в настоящее время изменила тяжелый прогноз рака пищевода».
Писал: «Введение высокой энергии в терапию ничем не оправдывает неразумных надежд. Речь не идет и не может идти о терапевтической революции. Можно просто надеяться, что практические преимущества этих лучей позволяют: 1) лечить некоторые формы рака, считавшиеся до сих пор рентгеноустоичивыми, так как нельзя было подать на них достаточную дозу,
2) улучшить статистические результаты, получаемые при рентгеноизлечимом раке, благодаря увеличению локальной дозы и объема мишени, наконец, меньшему изменению соседних тканей и общего состояния больного,
3) разработать в большом масштабе показания к паллиативному лечению больных, имеющих удовлетворительное общее состояние и способных перенести облучение без лучевой болезни».
Заключая свою работу, сообщил, что «для всех изученных локализации непосредственные результаты превосходны и использование высокоэнергетических лучей представляет с этой точки зрения большой шаг вперед. Местная и общая переносимость хорошая даже при сильных дозах и больших объемах. Отсутствие лучевой болезни, сохранение общего состояния больного облегчают задачу радиотерапевта и проведение намеченного лечения. Паллиативный эффект всегда достигался, и больной в конце лечения чувствовал улучшение. Нельзя еще окончательно оценить значение этих фактов для отдаленных результатов, которые остаются скромными; при любой локализации частота рецидива, местного или отдаленного, остается значительной...».
У нас в стране первая работа о применении излучений бетатрона 25 Мэв для лечения злокачественных опухолей опубликована в 1960 г. К- Н. Зиверт.
В 1964 г. Б. А. Цыбульский и И. И. Корнев сообщили о лучевом лечении на бетатроне 25 Мэв рака пищевода и кардиального отдела желудка. Они разработали методы продольного облучения опухоли в таком органе, как пищевод, и получили вполне удовлетворительные непосредственные результаты.
К настоящему времени опыт лечения больных раком пищевода лучами высоких энергий еще невелик. Не установлены разовые и суммарные дозы на очаг, которые привели бы к гибели все раковые клетки; не выяснено, с какой интенсивностью следует вести облучение опухоли и в какое время, для того чтобы не получить ее перфорации и т. д. В то же время известно, что данные лучи хорошо переносятся больными, не вызывают лучевую болезнь и дают несколько лучший непосредственный эффект по сравнению с классической рентгенотерапией. Можно надеяться, что дальнейшее изучение этого вопроса, особенно в клинико-биологическом направлении, а также техническое усовершенствование аппаратов будет способствовать постепенному улучшению терапевтического эффекта.
Хирурги, выполняющие резекцию пищевода при раке, считают, что их метод лечения более радикален, так как дает большее число случаев 5-летних выживаний по сравнению с лучевой терапией. Например, у С. В. Гейнаца и В. П. Клещевниковой 13,8% радикально оперированных больных пережили 5 лет и больше, у Б. А. Петрова— 21,5%, у Аёатз —22,5%.
Сторонники лучевой терапии доказывают, что этот метод лечения рака пищевода вряд ли уступает хирургическому, так как при лучевой терапии не наблюдается высокой смертности во время облучения, в то время как у хирургов имеется в среднем до 35% послеоперационных неудач. Кроме того, лучевому методу лечения подвергаются в основном те больные, которых хирурги отказались лечить.
Л. М. Гольдштейн, М. Н. Быченкова и Л. И. Залесская пишут: «Сопоставление результатов оперативного и лучевого лечения больных раком шейного и верхних двух третей грудного отдела пищевода позволяет рассматривать лучевую терапию как основной способ лечения этих больных», несмотря на то что, по данным этих авторов, из 149 длительно прослеженных после лучевой терапии больных больше года прожило только 29,5%.
Также провели сравнительную оценку хирургического и лучевого методов лечения больных раком пищевода. Они установили, что в облученной группе в 1-й год было больше выживших больных, а на 2-й год и позже — меньше по сравнению с группой оперированных. Авторы подчеркивали, что «облученная группа охватывает только неоперабельных больных, а если включить небольшие, ранние, опухоли, то результаты будут лучше».
По мнению «Хирургия в опытных руках является методом выбора для операбельных больных. Так как большинство опухолей не операбельно, единственно возможное лечение — рентгенотерапия».
Знакомство с работами сторонников лучевой терапии позволяет отметить, что некоторые из них отдаленные результаты подсчитывают не только к числу закончивших курс лечения, но и к количеству клинически излеченных больных (ВизсЬке, СапТгП, А. И. Рудерман и др.), что до некоторой степени может соответствовать данным хирургов, которые процент 5-летних излечений вычисляют на число больных, выписавшихся после операции резекции пищевода.
Нельзя полностью согласиться с тем, что лучевому лечению подвергаются только неоперабельные больные. К этому виду лечения также есть свои показания и противопоказания. У А. И. Рудермана, например, лучевой терапии подвергаются больные: 1) с достоверно установленным диагнозом, 2) при отсутствии отдаленных метастазов, 3) с ограниченной протяженностью опухолевого поражения и 4) при удовлетворительном общем
Состоянии. Показания А. И. Рудермана мало отличаются от показаний к производству резекции пищевода.
По сообщению «Тщательное сравнение всех опубликованных с 1937 г. результатов с 5-летним наблюдением леченных обоими способами (при гистологически установленном раке) дают нам показатель выживаемости в 1—2% при лучевой терапии и от 10 до 15% после успешной радикальной операции».
Таким образом, сравнение результатов лучевого и хирургического лечения свидетельствует о большей радикальности оперативного удаления рака пищевода. Тем не менее в настоящее время ни тот, ни другой метод лечения больных раком пищевода не дает вполне удовлетворительных результатов. В связи с этим появились предложения применять комбинированный — лучевой и хирургический — метод лечения этих больных. Сторонниками такой комбинированной терапии выступили с соавторами, Б. С. Розанов и А. И. Рудерман, В. П. Шакирова, , Стенопе соавторами и др.
С соавторами наблюдали две большие группы больных: одну—леченных хирургическим путем, другую— лучевым методом, причем во второй группе у ряда больных (9) была применена лучевая терапия до или после операции. На основании своего опыта авторы высказываются за сочетание обоих методов лечения у больных раком пищевода.
А. И. Рудерман считает, что при раке пищевода должно проводиться предоперационное облучение, имеющее целью: «1) устранение сопутствующих неспецифических воспалительных явлений как в самой опухоли, так и вокруг нее; 2) уменьшение опухоли и лимфатических узлов в результате повреждения наиболее чувствительных клеток; 3) развитие соединительной ткани и инкапсуляции оставшихся раковых гнезд в лимфатических узлах; 4) облитерацию мелких сосудов и лимфатических путей, гиалинизацию стенок артериол, т. е. понижение васкуляризации всей стромы опухоли... Если в результате проведения неполного курса облучения опухоль уменьшилась, а указанные симптомы исчезли, то при отсутствии противопоказаний целесообразна операция».
Выступая за комбинирование облучения и хирургического лечения, предпочитают также лучевую терапию как первый метод. Свою тактику в лечении больных Стенопе объясняет так: «Количество облучения, убивающее опухоль, иногда, а возможно и всегда, создает жизненно важное повреждение спинному мозгу. Такие изменения могут проявиться не ранее 6 месяцев после лечения. Это заставляет сократить общую дозу облучения и добавить хирургическую процедуру, чтобы закончить терапевтическое искоренение опухоли». Других указаний на повреждение спинного мозга после лучевой терапии рака пищевода нам в литературе встретить не удалось.
Некоторые авторы из-за возможной перфорации опухоли пищевода после применения дооперационного облучения предлагали сначала удалить опухоль, а в послеоперационном периоде произвести облучение оставшихся лимфатических узлов, тоже предпочитает применение высоковольтной терапии в послеоперационном периоде на область медиастинальных лимфатических узлов.
Большинство авторов высказывается за предоперационное облучение. Имеются разультаты комбинированного лечения, основанные на значительном количестве наблюдений.
Так, Хуан Куочжуэнь с соавторами у 113 больных с опухолью средней трети пищевода провели телекобальтовое облучение (доза от 100 до 4500 уг). Через 10 дней после окончания облучения у 80 больных опухоль удалось резецировать, 33 были неоперабельными. Общая резектабельность была на 12,4% больше, чем в контрольной группе. «Повышение резектабельности при комбинированном предоперационном облучении и хирургическом вмешательстве связано с наступающим уменьшением размеров опухоли и замещением раковой инфильтрации фиброзной тканью», — пишут авторы.
Очень интересные данные представили с соавторами. С целью улучшить отдаленные результаты лечения больных раком пищевода они в течение уже нескольких лет проводят работу по комбинированному лечению рака пищевода. Сначала выполняется лучевая терапия малыми дозами (2000—3000 г за 10—14 дней). Для облучения используют установку 2000 кюри к теле-
Применяют вращательное облучение, по окончании которого немедленно производят операцию. По такому методу лечили 114 больных. Авторы отметили увеличение операбельности и улучшение отдаленных результатов по сравнению с группой больных, леченных только хирургическим путем.
С мая 1962 г. с сотрудниками изменили методику предоперационного облучения. Общую дозу в 2000 г применяли в течение 3 дней: 700, 700 и 600 г. Через 4—7 дней по окончании облучения выполнялась операция. Авторы отмечают, что при таком облучении «мало фракционированным кратковременным методом» избирательное лучевое действие на раковую ткань более отчетливо, чем при долгосрочном курсе. Кроме того, при коротком сроке облучения не так легко наступает перфорация опухоли. Всего указанным методом лечено 99 больных, у 22 из них был рак верхне-грудного и средне-грудного отделов пищевода.
В целом при комбинированном лечении рака верхних двух третей пищевода получил 44,4% 3-летнего выживания больных вместо 21,7% при чисто хирургическом и 6,8% при чисто лучевом лечении.
Приведенные результаты убедительно показывают преимущество комбинированного лечения — облучение малой дозой и операция — перед другими методами лечения рака пищевода.
К сожалению, такими результатами располагают единичные учреждения. В нашей стране комбинированное лечение рака пищевода до сих пор не получило широкого распространения. Между тем данные литературы свидетельствуют о том, что методы лечения злокачественных опухолей, в том числе и рака пищевода, следует комбинировать, включая и химиотерапию.