Клеточные имплантаты, генная терапия, даже оптогенетика делают успехи в клинических испытаниях для лечения различных форм слепоты.
В последние годы ученые достигли того, что раньше бы назвали чудом: они дали слепым пациентам возможность лучше видеть. В 2019 году область восстановления зрения значительно продвинулась благодаря генной терапии для коррекции потери зрения у некоторых пациентов с детской слепотой.
И только на прошлой неделе исследователи сообщили, что ретинальный имплантат позволил 69-летней женщине с дегенерацией желтого пятна более чем вдвое увеличить количество букв, которые она могла идентифицировать на карте зрения.
Имплантат, предоставленный пяти пациентам с сухой возрастной дегенерацией желтого пятна (AMD), представляет собой единый слой пигментных эпителиальных клеток сетчатки (RPE), полученных из эмбриональных стволовых клеток человека. Другие команды по всему миру придумывают свои собственные формы имплантатов RPE, и этот тип подхода является лишь одним из множества способов тестирования, которые либо замедляют, либо обращают вспять различные формы слепоты.
Клеточные имплантаты
В последнем исследовании по сухому ВМД, опубликованном 4 апреля в Science Translational Medicine, команда ученых и инженеров из Университета Южной Калифорнии (USC) в Лос-Анджелесе впервые дифференцировала эмбриональные стволовые клетки человека (ESCs) в клетки RPE - те, которые образуют монослой, который поддерживает здоровье лежащей в основе фоторецепторной сетчатки. Разложенные на крошечной полимерной платформе (всего 6 мм на 3 мм), клетки собирались в поляризованный монослой, точно такой же, как в человеческом глазу.
Чтобы вставить клетки, Кашани сделал разрез на 1 миллиметр в сетчатке, и с имплантатом, сложенным пополам, он сунул его в глаз и развернул его под сетчаткой - которая удерживает пластырь на месте - на верхней части поврежденной области.
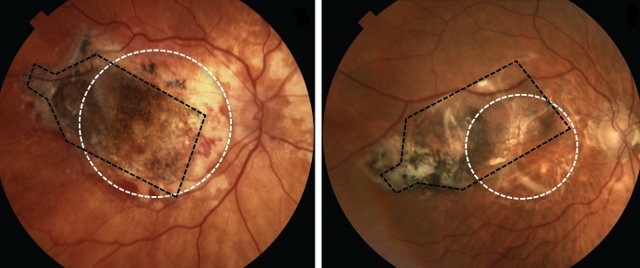
Три пациента увидели улучшения в течение трех месяцев после получения имплантата, в том числе один пациент, который мог прочитать дополнительные буквы на карте зрения. У двух других пациентов отмечалось улучшение фиксации, способность фокусировать взгляд на объекте.
Другой недавний подход, основанный на использовании стволовых клеток, исследователями из Великобритании позволил улучшить зрение у двух пожилых пациентов с влажной формой ВМД. В этих случаях сосуды глаза растут ненормально и приводят к кровотечению, разрушению клеток RPE и возможной слепоте. Разработчики также использовали покрытую синтетическую мембрану, на которой они собирали клетки RPE, дифференцированные от человека, и хирургически доставляли пластырь. Каждый пациент также имел поразительные улучшения в скорости чтения, с 1,7 до 82,8 и от 0 до 47,8 слов в минуту, соответственно.
Первая демонстрация того, что ЭСК человека, дифференцированные в клетки RPE, безопасны, была в 2012 году, когда Стивен Шварц из Калифорнийского университета в Лос-Анджелесе и его коллеги успешно ввели клетки RPE, полученные из ЭСК, двум слепым пациентам, один с сухой ВМД, а другой с макулярной дистрофией Старгардта, еще одним дегенеративным заболеванием глаз. В отчете о 18 пациентах за 2014 год команда вместе с производителем клеток Astellas Pharma показала, что у 10 пациентов наблюдалось улучшение зрения. Шварц и его коллеги в настоящее время планируют зарегистрировать более масштабное исследование, чтобы проверить, будет ли эффективным введение инъекций большего количества клеток RPE, полученных из ЭСК человека, чем в первоначальном исследовании.
Одной из проблем при использовании ЭСК человека является потенциальная иммунная реакция и последующее отторжение клеток как чужеродных. Для разработки индивидуальной клеточной терапии, получаемой из собственных клеток пациентов, группа в Японии во главе с Масайо Такахаши из Центра биологии развития RIKEN обратилась к перепрограммированию клеток из фибробластов кожи в индуцированные плюрипотентные стволовые (IPS) клетки, а затем в клетки RPE. Недавно ее команда показала, что у пациентки с AMD, у которой в глаза был имплантирован слой таких клеток RPE, не было никакой дополнительной атрофии зрения в течение года.
Есть также исследователи, работающие над более масштабируемым подходом, использующим донорские, сопоставимые с иммунитетом клетки IPS для лечения многих пациентов. Банк клеток IPS от различных доноров был бы гораздо более осуществимым, экономически эффективным и удобным, чем создание клеток IPS из собственных клеток каждого пациента.
Генная терапия и санатории
Чтобы исправить определенные генетические дефекты, связанные с нарушениями зрения, исследователи обратились к генной терапии - и достигли поразительных результатов. Генная терапия, одобренная FDA в прошлом году, исправляет мутацию, обнаруженную при врожденном амаврозе Лебера (LCA) - редкой, наследственной форме детской слепоты - и других формах наследственных дистрофий сетчатки, содержащих мутацию в гене RPE65 . Белок, кодируемый геном, является ферментом, необходимым для клеток сетчатки, чтобы генерировать зрительные пигменты. Эти наследственные расстройства обычно начинаются с ночной слепоты и могут прогрессировать до ухудшения периферического зрения, а затем полной потери зрения в детстве.
Другая генная терапия, все еще находящаяся в разработке, продуцирует белок, который блокирует активность фактора роста эндотелия сосудов (VEGF), и уже было доказано, что он безопасен и эффективен в ранних стадиях влажного клинического испытания AMD.
Изюминка генной терапии - это оптогенетический подход, при котором вектор, кодирующий канальродопсин из зеленых водорослей, доставляется в ганглиозные клетки сетчатки. Компания Allergan в настоящее время тестирует подход, разработанный Zhuo-Hua Pan, исследователем зрения в государственном университете Уэйна, на ранней стадии исследования для пациентов с пигментным ретинитом, в котором пациенты теряют светочувствительные клетки сетчатки. По словам Пэна, цель состоит в том, чтобы придать светочувствительность клеткам сетчатки, которые обычно не способны воспринимать свет. В то время как некоторые генные терапии, такие как одобренная для LCA, нацелены на специфический мутированный ген, оптогенетическая терапия может использоваться для лечения любой слепоты из-за потери фоторецепторных клеток, говорит Пан.
Санатории специализирующиеся на лечении органов зрения также предлагают действенные методы восстановления зрения, такие как глазной санаторий в Пятигорске.
Недоказанные подходы с использованием стволовых клеток
Генная и клеточная терапия находятся в стадии разработки и находятся на ранних стадиях, и пока что из небольшого числа пациентов, получавших лечение, пока не ясно, насколько широко они могут применяться к людям с потерей зрения. Тщательные клинические исследования этих технологий открывают путь к все более масштабным испытаниям, и есть клиники, продающие неутвержденные виды лечения клиентам со слепотой несмотря на то, что не существует методов лечения на основе стволовых клеток для лечения тяжелых заболеваний глаз.
Недавно три женщины, каждая с дегенерацией желтого пятна, получили лечение без проверенных стволовых клеток обоих глаз в клинике во Флориде. Все трое были постоянно ослеплены. Альбини говорит, что «Процедуру следует проводить только над одним глазом», в то время как клиника стволовых клеток во Флориде проводила терапию для обоих глаз, ослепляя женщин на двусторонней основе.
Несмотря на плохую репутацию мошенников, исследователи офтальмологии настроены оптимистично по поводу того, что принесут новые методы лечения и достижения в ближайшие десятилетия.